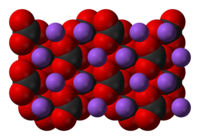
Carbonato de sodio
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Carbonato sódico?
Resumir este artículo para un niño de 10 años
El carbonato de sodio o carbonato sódico es una sal blanca y translúcida de fórmula química Na2CO3, usada entre otras cosas en la fabricación de jabón, vidrio y tintes. Es conocido comúnmente como barrilla, natrón, sosa Solvay, soda Solvay, sosa Ash, ceniza de soda y carbonato sódico anhidro[1] o simplemente sosa, (no se ha de confundir con la sosa cáustica, que es el hidróxido de sodio, un derivado del carbonato sódico, obtenido mediante un proceso conocido como caustificación o por electrólisis). Es la sustancia alcalina más común que se conoce y utiliza desde la antigüedad.[4] Tiene una alta absorción de humedad. Se disuelve fácilmente en agua para formar una solución acuosa de alcalinidad media. el carbonato de sodio es ampliamente utilizado en varios campos de todo el mundo. Una de las aplicaciones más importantes del carbonato de sodio es para la fabricación de vidrio. Según las estadísticas, alrededor de la mitad de la producción total de carbonato de sodio se utiliza para fabricar vidrio. En el proceso de producción de vidrio, el carbonato de sodio desempeña un papel de flujo en el proceso de fusión de sílice.[5]
 | ||
 | ||
| Nombre IUPAC | ||
| Trioxocarbonato(IV) de Sodio | ||
| General | ||
| Otros nombres |
Barrilla natrón sosa Solvay ceniza de soda E-500 sosa calcinada soda ash cristales de soda xoda lavada carbonato sódico anhidro[1] | |
| Fórmula estructural |
 | |
| Fórmula molecular | Na2CO3 | |
| Identificadores | ||
| Número CAS | 497-19-8[2] | |
| Número RTECS | VZ4050000 | |
| ChEBI | 29377 | |
| ChEMBL | CHEMBL186314 | |
| ChemSpider | 9916 | |
| DrugBank | 09460 | |
| PubChem | 10340 | |
| UNII | 45P3261C7T | |
| Propiedades físicas | ||
| Apariencia | Sólido blanco[3] | |
| Densidad | 2540 kg/m³; 2,54 g/cm³ | |
| Masa molar | 105,9885 g/mol | |
| Punto de fusión | 1124 K (851 °C) | |
| Punto de ebullición | 1873 K (1600 °C) | |
| Propiedades químicas | ||
| Acidez | 10,33 pKa | |
| Solubilidad en agua | 30.7 g por cada 100 g de agua (25 °C) | |
| Termoquímica | ||
| ΔfH0líquido | -1102 kJ/mol | |
| ΔfH0sólido | -1131 kJ/mol | |
| S0sólido | 135 J·mol–1·K–1 | |
| Peligrosidad | ||
| SGA |
 | |
| NFPA 704 |
0
1
1
| |
| Frases R | R36 | |
| Frases S | (S2), S22, S26 | |
| Frases H | H319 | |
| Frases P | (P260), (P305 + P351 + P338) | |
| Riesgos | ||
| Ingestión | Causa irritación y diarrea sangrante. | |
| Inhalación | Dañina, deben evitarse especialmente exposiciones prolongadas. | |
| Piel | Irritaciones y posiblemente quemaduras. | |
| Ojos | Irritación grave, posiblemente con heridas graves.[3] | |
| Compuestos relacionados | ||
| Otros aniones | Bicarbonato de sodio | |
| Otros cationes |
Carbonato de litio Carbonato de potasio | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Puede hallarse en la naturaleza u obtenerse artificialmente, gracias a un proceso ideado y patentado en 1791 por el médico y químico francés Nicolás Leblanc. El proceso Leblanc implicaba las siguientes reacciones químicas:
- Reacción de sal común con ácido sulfúrico: 2 NaCl + H2SO4 → Na2SO4 + 2 HCl
- Reacción de calcinación de Na2SO4 con caliza y carbón: Na2SO4 + CaCO3 + 2 C → Na2CO3 + CaS + 2 CO2[4]
Más adelante este método fue sustituido por el método Solvay ideado por el químico belga Ernest Solvay. Solvay fundó en 1863 la compañía Solvay donde utilizó profusamente su método que conseguía abaratar aún más el proceso y eliminar algunos de los problemas que presentaba el método Leblanc. Este método utiliza como materias primas el cloruro de sodio (sal común), el amoníaco y el carbonato de calcio (piedra caliza). En 1915 se cerró la última fábrica de sosa Leblanc.[4]