Énolase
famille InterPro / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Énolase?
Résumez cet article pour un enfant de 10 ans
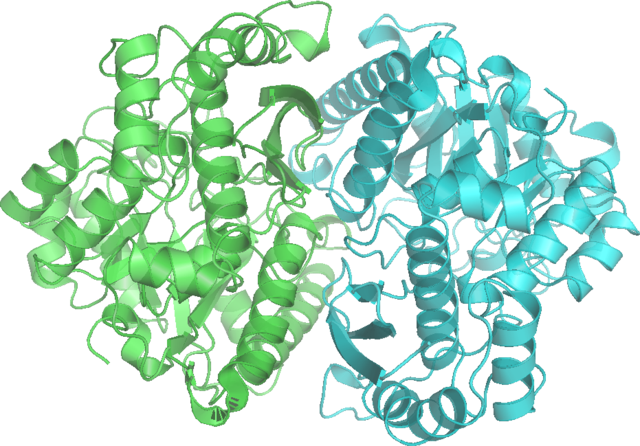
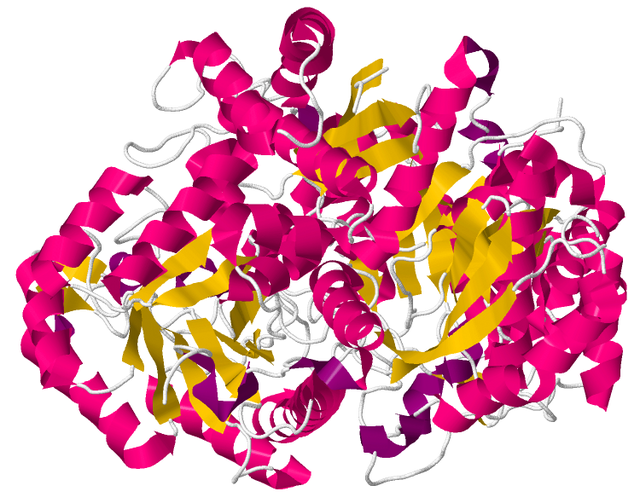
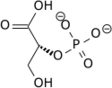
L'énolase, également connue sous les noms de phosphopyruvate hydratase ou 2-phosphoglycérate déshydratase, est une métalloenzyme responsable de la catalyse qui convertit le 2-phospho-D-glycérate (2PG) en phosphoénolpyruvate (PEP), la 9e et avant-dernière étape de la glycolyse :
 |
 H2O + H2O + |
 |
| 2-phosphoglycérate | Phosphoénolpyruvate |
| Énolase 1 | ||
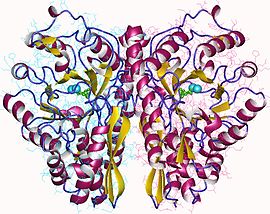 Homodimère d'énolase de levure complexée avec un mélange à l'équilibre de 2PG et de PEP (PDB 1ONE[1]). | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | ENO1 | |
| N° EC | 4.2.1.11 | |
| Homo sapiens | ||
| Locus | 1p36.23 | |
| Masse moléculaire | 47 169 Da[2] | |
| Nombre de résidus | 434 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| Énolase 2 (neuronale) | ||
| Caractéristiques générales | ||
| Symbole | ENO2 | |
| N° EC | 4.2.1.11 | |
| Homo sapiens | ||
| Locus | 12p13.31 | |
| Masse moléculaire | 47 269 Da[2] | |
| Nombre de résidus | 434 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| Énolase 3 (musculaire) | ||
| Caractéristiques générales | ||
| Symbole | ENO3 | |
| N° EC | 4.2.1.11 | |
| Homo sapiens | ||
| Locus | 17p13.2 | |
| Masse moléculaire | 46 987 Da[2] | |
| Nombre de résidus | 434 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
| Énolase 4 | ||
| Caractéristiques générales | ||
| Symbole | ENO4 | |
| N° EC | 4.2.1.11 | |
| Homo sapiens | ||
| Locus | 10q25.3 | |
| Masse moléculaire | 68 821 Da[2] | |
| Nombre de résidus | 628 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
L'énolase appartient à la classe de lyases. L'énolase peut aussi catalyser la réaction inverse, selon les concentrations du substrats dans le milieu[3]. Le pH optimal pour cette enzyme est de 6,5[4]. L'énolase est présente dans tous les tissus et organismes capables de réaliser la glycolyse ou la fermentation. L'enzyme a été découverte par Lohmann et Meyerhof en 1934[5] et a depuis été isolée au sein de divers organes sources tels que le muscle humain et les érythrocytes[4].
| N° EC | EC 4.2.1.11 |
|---|---|
| N° CAS | 9014-08-8 |
| Cofacteur(s) | Magnésium |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |