
Klorát
From Wikipedia, the free encyclopedia
A klorát a ClO−3 anion elterjedt neve, ahol a klór oxidációs száma 5. Az elnevezés utalhat a klorátiont tartalmazó vegyületekre is – a klorátok a klórsav sói és észterei. A klór többi oxoanionjának szabályos neve „klorát”, melyet zárójelben a klór oxidációs száma követ zárójelben, például a perklorát (ClO−4) esetén klorát(VII).
| Klorát | |||
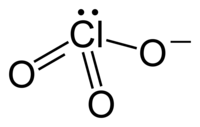 Szerkezete és kötései | |||
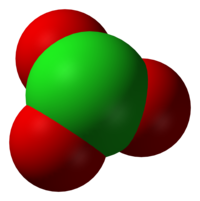 A klorátion | |||
| Más nevek | Klorát(V) | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 14866-68-3 | ||
| PubChem | 104770 | ||
| ChemSpider | 94578 | ||
| ChEBI | 49709 | ||
| |||
| InChIKey | XTEGARKTQYYJKE-UHFFFAOYSA-M | ||
| Gmelin | 1491 | ||
| UNII | 08Z8093742 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | ClO3- | ||
| Moláris tömeg | 83,4512 g/mol | ||
| Kristályszerkezet | |||
| Molekulaforma | Trigonális piramis | ||
| Veszélyek | |||
| Főbb veszélyek | oxidáns | ||
| Rokon vegyületek | |||
| Azonos kation |
| ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A vegyértékelektronpár-taszítási elméletnek megfelelően a klorátionok trigonális piramis alakúak.
A klorátok erős oxidálószerek, és szerves anyagoktól vagy könnyen oxidálható anyagoktól távol tartandók. A klorátok éghető anyaggal (például cukorral, fűrészporral, szénnel, szerves oldószerekkel, fémekkel) való keveréke könnyen deflagrálhat. Egykor pirotechnikai célra is használták ezért, de instabilitásuk miatt a stabilabb perklorátokat használják helyettük.