
Peróxido de hidrogênio
composto químico / De Wikipedia, a enciclopédia encyclopedia
O peróxido de hidrogénio (português europeu) ou peróxido de hidrogênio (português brasileiro) que, em solução aquosa, é conhecido comercialmente como água oxigenada, é um líquido claro de fórmula química H2O2. Foi descrito a primeira vez por Louis Jacques Thénard, numa reacção de peróxido de bário com ácido nítrico.[1]
| Fórmula estrutural | |
|---|---|
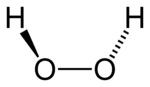
| |
| Geral | |
| Nome IUPAC | Peróxido de hidrogênio |
| Nomes usuais | Água oxigenada peróxido de di-hidrogênio dióxido de diidrogênio |
| Fórmula química | H2O2 |
| Massa molar | 34.01475 g/mol |
| Aparência | Líquido claro |
| Número do CAS | 7722-84-1 |
| Comportamento de fase | |
| Ponto de fusão | 262 K (-11°C) |
| Ponto de ebulição | 414 K (141°C) |
| Propriedades sólidas | |
| ΔfH0sol | -200 kJ kJ/mol |
| S0sol | ? J/mol·K |
| Propriedades líquidas | |
| Densidade | 1,476 g/cm³ |
| Solubilidade em água | miscível |
| Viscosidade | 1,245 cP a 20°C |
| ΔfH0liq | -188 kJ/mol |
| S0liq | 110 J/mol·K |
| Propriedades gasosas | |
| ΔfH0liq | -136,11 kJ/mol |
| S0liq | 232,95 J/mol·K |
| Segurança | |
| Símbolos de risco | |
 C Corrosivo | |
| Instruções de Risco e Segurança | R: 34 S: 3-26-36/37/39-45 |
| Ponto de fulgor | não inflamável |
| Ingestão | Problemas sérios, possível morte. |
| Inalação | Irritação severa. Possível morte. |
| Mais informações | |
| MSDS | Hazardous Chemical Database |
| Unidades do SI são usadas quando possível. Salvo quando especificado o contrário, são considerados condições normais de temperatura e pressão. | |
Trata-se de um líquido viscoso e poderoso oxidante. É incolor à temperatura ambiente e apresenta característico sabor amargo. Quantidades pequenas de peróxido de hidrogénio gasoso ocorrem naturalmente no ar. O peróxido de hidrogénio é instável e, quando perturbado, rapidamente se decompõe (através da enzima catalase, presente em nosso corpo), de H2O2, em água (H2O) e oxigênio (O2) com liberação de calor. Deste modo, quando ele é transformado em água e oxigénio pela catalase, acaba por matar bactérias e vírus anaeróbicos (que não sobrevivem à presença de oxigénio), pois libera oxigénio puro, tendo a função de desinfectante oxidante. Embora não seja inflamável, é poderoso agente oxidante que pode sofrer combustão espontânea em contacto com matéria orgânica, alguns metais como o cobre ou algumas ligas metálicas como o bronze.
O peróxido de hidrogénio actua ainda em diversos mecanismos de degradação de aminoácidos (em associação com amino-oxidases), por conta de seu poder oxidante elevado. Tal composto ainda pode actuar na fotossíntese (ciclo do glioxilato), e na síntese de glicose a partir de fontes que não contenham carboidratos (gliconeogénese).


