Chiralita (chémia)
From Wikipedia, the free encyclopedia
V chémii sa molekula nazýva chirálnou, pokiaľ nie je možné ju zjednotiť s jej zrkadlovým obrazom žiadnou kombináciou rotácií, translácií alebo nejakými konformačnými zmenami. Táto geometrická vlastnosť sa označuje ako chiralita.[1][2][3][4][5] Tento pojem pochádza zo starogréckeho είρ (cheir), „ruka“, čo je bežný príklad objektu s touto vlastnosťou.

Chirálna molekula existuje v podobe dvoch stereoizomérov, ktoré sú vzájomne zrkadlovými obrazmi. Tieto stereoizoméry sa nazývajú enantioméry – často sa rozlišujú ako „pravotočivý“ alebo „ľavotočivý“ podľa ich absolútnej konfigurácie alebo iného kritéria. Dva enantioméry majú rovnaké chemické vlastnosti, okrem ich reaktivity s inými chirálnymi zlúčeninami. Majú zároveň i zhodné fyzikálne vlastnosti, okrem toho, že majú často opačnú optickú aktivitu. Optická aktivita enantiomérov však môže byť veľmi nízka, čo sa potom označuje ako kryptochiralita. Homogénna zmes dvoch enantiomérov v rovnakom pomere sa nazýva racemát a zvyčajne sa líši (chemicky i fyzikálne) od čistých enantiomérov.
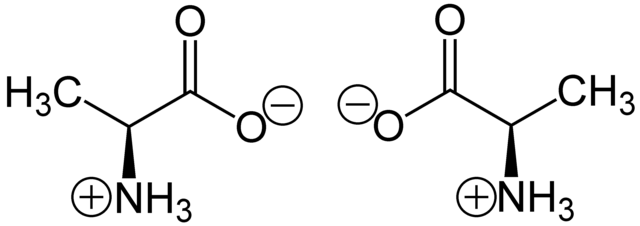
Chirálne molekuly majú zvyčajne stereogénny prvok, na základe ktorého chiralita vzniká. Najbežnejší typ stereogénneho prvku je stereogénne centrum (stereocentrum). V prípade organických zlúčenín sú to typicky uhlíkové atómy, na ktorých sú v tetraédrickej geometrii naviazané štyri rôzne skupiny. Pre dané stereocentrum sú dva spôsoby, ktorými je možné tieto skupiny naviazať, čím vznikajú stereoizoméry (diastereoméry a enantioméry) u molekúl s viac než jedným stereocentrom. U chirálnych molekúl s jedným alebo viacerými stereocentrami odpovedá enantioméru ten stereoizomér, v ktorom majú všetky stereocentrá opačnú konfiguráciu. Inak povedané, pre konkrétnu molekulu má pár enantiomérov opačné konfigurácie na všetkých stereocentrách. Organická zlúčenina, ktorá má len jeden stereogénny uhlík, je vždy chirálna. Oproti tomu sú zlúčeniny, ktoré majú viac stereogénnych uhlíkov, zvyčajne ale nie vždy chirálne. Totiž, ak sú stereocentrá usporiadané tak, že molekula má vnútornú rovinu symetrie, tak je molekula achirálna a označuje sa ako mezozlúčenina. Ostatné atómy, napríklad N, P, S alebo Si, môžu byť takisto stereocentrami, ak sú na nich naviazané štyri rôzne substituenty (vrátane voľného elektrónového páru).
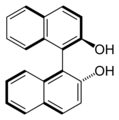
Molekuly, ktorých chiralita pochádza z prítomnosti jedného alebo viacerých stereocentier, majú centrálnu chiralitu. Existujú ešte dva druhy stereogénnych prvkov, ktoré môžu viesť k chiralite: stereogénna os (axiálna chiralita) a stereogénna rovina (planárna chiralita). Posledným spôsobom, ktorým môže byť molekula chirálna, je kvôli jej prirodzenému zakriveniu v priestore (inherentná chiralita). Tieto druhy chirality sú však omnoho menej časté, než centrálna chiralita. BINOL je typický príklad axiálne chirálnej molekuly a trans-cyklooktén je bežný príklad planárne chirálnej molekuly. Helicén má helikálnu chiralitu, čo je jeden z druhov inherentnej chirality.
- (R) enantiomér BINOLu, príklad axiálnej chirality.
- Dva enantioméry trans-cyklookténu, príklad planárnej chirality.
- 10-Helicén, ktorý má helikálnu štruktúru a teda je inherentne chirálny.
Chiralita je dôležitý koncept v stereochémii a biochémii. Väčšina zlúčenín, ktoré sú dôležité v biológii, je chirálna, napríklad sacharidy (cukry, škrob a celulóza), aminokyseliny, z ktorých sa skladajú bielkoviny, a nukleové kyseliny. V živých organizmoch sa typicky nachádza len jeden z dvoch enantiomérov chirálnej zlúčeniny. Z tohto dôvodu vedia organizmy, ktoré prijímajú chirálne zlúčeniny, spracovať zvyčajne len jeden z jeho enantiomérov. Z toho istého dôvodu majú dva enantioméry chirálneho liečiva veľmi rozdielne účinky alebo silu.
Chiralita je vnútorná vlastnosť identity molekuly, takže systematický názov musí zahŕňať detaily jej absolútnej konfigurácie (R/S, D/L alebo iné deskriptory).