யூரியா
From Wikipedia, the free encyclopedia
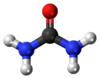
யூரியா (Urea) என்பது CO(NH2)2 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கரிம வேதியியல் சேர்மமாகும். கார்பமைடு என்ற பெயராலும் இது அழைக்கப்படுகிறது. அமைடு மூலக்கூறில் இரண்டு அமீன் ( –NH2) குழுக்கள் ஒரு கார்பனைல் (C=O) வேதி வினைக்குழுவால் இணைக்கப்பட்டிருக்கும்.
| |||
| |||
| பெயர்கள் | |||
|---|---|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
யூரியா[1] | |||
| முறையான ஐயூபிஏசி பெயர்
கார்பானிக் டையமைடு[1] | |||
| வேறு பெயர்கள்
கார்பமைடு கார்பனைல் டையமைடு கார்பனைல் டையமீன் டையமினோமெத்தனால் டையமினோமெத்தனோன் | |||
| இனங்காட்டிகள் | |||
| 57-13-6 | |||
Beilstein Reference |
635724 | ||
| ChEBI | CHEBI:16199 | ||
| ChEMBL | ChEMBL985 | ||
| ChemSpider | 1143 | ||
| DrugBank | DB03904 | ||
Gmelin Reference |
1378 | ||
IUPHAR/BPS |
4539 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| KEGG | D00023 | ||
| பப்கெம் | 1176 | ||
| வே.ந.வி.ப எண் | YR6250000 | ||
| |||
| UNII | 8W8T17847W | ||
| பண்புகள் | |||
| CH4N2O | |||
| வாய்ப்பாட்டு எடை | 60.06 g·mol−1 | ||
| தோற்றம் | வெண் திண்மம் | ||
| அடர்த்தி | 1.32 கிராம்/செ.மீ3 | ||
| உருகுநிலை | 133 முதல் 135 °C (271 முதல் 275 °F; 406 முதல் 408 K) | ||
| 1079 கிராம்/லிட்டர் (20 °செல்சியசு) 1670 கிராம்/லிட்டர் (40 °செல்சியசு) 2510 கிராம்/லிட்டர் (60 °செல்சியசு 4000 கிராம்/லிட்டர் (80 °செல்சியசு) | |||
| கரைதிறன் | 500 கிராம்/லிட்டர் கிளிசரால்[2]
50 கிராம்/லிட்டர் எத்தனால் | ||
| காரத்தன்மை எண் (pKb) | 13.9[4] | ||
| -33.4•10−6 செ.மீ3/மோல் | |||
| கட்டமைப்பு | |||
| இருமுனைத் திருப்புமை (Dipole moment) | 4.56 D | ||
| வெப்பவேதியியல் | |||
| Std enthalpy of formation ΔfH |
-333.19 கிலோயூல்/மோல் | ||
| தீங்குகள் | |||
| பொருள் பாதுகாப்பு குறிப்பு தாள் | JT Baker | ||
| GHS pictograms |  | ||
| தீப்பற்றும் வெப்பநிலை | தீப்பற்றாது | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (Median dose) |
8500 மி.கி/கி.கி (வாய்வழி, எலி) | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
நைட்ரசன் அடங்கிய சேர்மங்களை விலங்குகள் செரிக்கும்போது அவற்றின் வளர்சிதை மாற்றத்தில் யூரியா முக்கிய பங்கு வகிக்கிறது. இதுவே பாலூட்டிகளின் சிறுநீரில் கலந்திருக்கும் நைட்ரசன் உள்ள முதன்மையான பொருளாகும். யூரியா நிறமற்றும் நெடியற்றும் உள்ள திண்மமாகும். நீரில் இது நன்றாகக் கரையும். நடைமுறையில் பொதுவாக யூரியா நச்சுத்தன்மையற்று காணப்படுகிறது. எலிகளில் இதன் உயிர் கொல்லும் அளவு கிலோகிராமுக்கு 15 கிராம் மட்டுமேயாகும் [5]. நீரில் கரைந்திருக்கும்போது இது காடியாவோ காரமாகவோ இருப்பதில்லை. விலங்கு உடலானது யூரியாவை பல செயல்முறைகளில் பயன்படுத்திக் கொள்கிறது. பின்னர் குறிப்பாக நைட்ரசன் கழிவாக வெளியேற்றுகிறது. கல்லீரலில் நடைபெறும் யூரியா சுழற்சியின் போது இரண்டு அமோனியா ((NH3)) மூலக்கூறுகளுடன் ஒரு கார்பனீராக்சைடு (CO2) மூலக்கூறு சேர்ந்து யூரியா தயாரிக்கப்படுகிறது. உரங்களில் ஒரு நைட்ரசன் (N) மூலப்பொருளாக பரவலாகப் பயன்படுத்தப்படுகிறது. வேதித் தொழிற்சாலைகளில் ஒரு தாதுப் பொருளாகவும் யூரியா முக்கியத்துவம் பெறுகிறது.
1828 ஆம் ஆண்டு பிரடெரிக் வோலர் கனிமச் சேர்மங்களிலிருந்து செயற்கை முறையில் யூரியாவை தயாரித்தது வேதியியல் துறையில் ஒரு முக்கியமான மைல் கல்லாகும். முன்னதாக ஓர் உடன் விளைபொருளாக மட்டுமே அறியப்பட்ட யூரியா என்ற வேதிப்பொருள் உயிரியல் தொடக்கப் பொருட்கள் இல்லாமல் ஆய்வகத்தில் செயற்கை முறையில் ஒருங்கிணைத்து தயாரிக்க முடியும் என்பதை இக்கண்டுபிடிப்பு முதன்முறையாகக் காட்டியது. பரவலாக நம்பப்பட்டுவந்த உயிர்வாழும் கோட்பாட்டிற்கு முரணாகவும் இது அமைந்தது.