
Enllaz metálicu
From Wikipedia, the free encyclopedia
Un enllaz metálicu ye un enllaz químicu que caltién xuníos los átomos (unión ente nucleos atómicos y los electrones de valencia, que se xunten alredor d'éstos como una nube) de los metales ente sigo.[1]
Esti artículu o seición necesita referencies qu'apaezan nuna publicación acreitada, como revistes especializaes, monografíes, prensa diaria o páxines d'Internet fiables. |
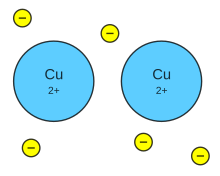
Estos átomos arrexuntar de forma bien cercana unos a otros, lo que produz estructures bien compactes. Trátase de llinies tridimensionales qu'adquieren estructures tales como: la típica d'empaquetamiento compactu d'esferes (hexagonal compacta), cúbica centrada nes cares o la cúbica centrada nel cuerpu.
Nesti tipu d'estructura cada átomu metálicu ta estremáu por otros dolce átomos (seis nel mesmu planu, trés percima y trés per debaxo). Amás, por cuenta de la baxa electronegatividá que tienen los metales, los electrones de valencia son estrayíos de les sos orbitales. Esti enllaz namái puede tar en sustancies en estáu sólidu.[2]
Los metales tienen delles propiedaes carauterístiques que los estremen de los demás materiales. Suelen ser sólidos a temperatura ambiente, sacante'l mercuriu, y tienen un puntu de fusión alto.
L'enllaz metálicu ye carauterísticu de los elementos metálicos. Ye un enllaz fuerte, primariu, que se forma ente elementos de la mesma especie. Al tar los átomos tan cercanos unos d'otros, interaccionan los sos nucleos xunto coles sos nubes electróniques, empaquetándose nos trés dimensiones, polo que queden los nucleos arrodiaos de tales nubes. Estos electrones llibres son los responsables de que los metales presenten una elevada conductividá llétrica y térmica, una y bones estos puédense mover con facilidá si se pon en contautu con una fonte llétrica. Los metales xeneralmente presenten rellumu y son maleables.
Los elementos con un enllaz metálicu tán compartiendo un gran númberu d'electrones de valencia, formando un mar d'electrones arrodiando un enrexáu xigante de cationes.[3]
Munchos de los metales tienen puntos de fusión más altos qu'otros elementos non metálicos, polo que puede inferise qu'hai enllaces más fuertes ente los distintos átomos que los componen.
La vinculación metálica ye non polar, apenes hai diferencia d'electronegatividá ente los átomos que participen na interacción de la vinculación (nos metales, elementales puros) o bien poca (nes aleaciones), y los electrones implicaos no que constitúi la interacción al traviés de la estructura cristalina del metal. L'enllaz metálicu esplica munches carauterístiques físiques de metales, tales como maleabilidá, ductilidá, bonos na conducción de calor y lletricidá, y con rellumo o llustre (devuelven la mayor parte de la enerxía llumínica que reciben).
La vinculación metálica ye l'atracción electrostática ente los átomos del metal o cationes y los electrones deslocalizados. Esta ye la razón pola cual puede esplicase un deslizamiento de capes, dando por resultancia la so carauterística maleabilidá y ductilidá.
Los átomos del metal tienen a lo menos un electrón de valencia, nun comparten estos electrones colos átomos vecinos, nin pierden electrones pa formar los iones. Nel so llugar los niveles d'enerxía esternos de los átomos del metal se traslapan. Son como enllaces covalentes identificaos.