অ্যাসিটোন
রাসায়নিক যৌগ / From Wikipedia, the free encyclopedia
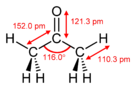
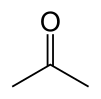
অ্যাসিটোন বা প্রোপানন একটি জৈব যৌগ, যার রাসায়নিক সংকেত (CH3)2CO।[15] এটি ক্ষুদ্রতম ও সরলতম কিটোন। এটি বর্ণহীন, অত্যন্ত উদ্বায়ী, দাহ্য এবং তীব্র গন্ধযুক্ত পদার্থ।
| |||
| |||
 | |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নাম
Acetone[2] | |||
| পছন্দসই ইউপ্যাক নাম
Propan-2-one[3] | |||
| অন্যান্য নাম | |||
| শনাক্তকারী | |||
| |||
ত্রিমাত্রিক মডেল (জেমল) |
|||
| থ্রিডিমেট | |||
| বেইলস্টেইন রেফারেন্স | 635680 | ||
| সিএইচইবিআই | |||
| সিএইচইএমবিএল | |||
| কেমস্পাইডার |
| ||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৬০২ | ||
| ইসি-নম্বর |
| ||
| মেলিন রেফারেন্স | 1466 | ||
| কেইজিজি |
| ||
| এমইএসএইচ | Acetone | ||
পাবকেম CID |
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই | |||
| ইউএন নম্বর | 1090 | ||
কম্পটক্স ড্যাশবোর্ড (EPA) |
|||
| |||
এসএমআইএলইএস
| |||
| বৈশিষ্ট্য | |||
| C3H6O | |||
| আণবিক ভর | ৫৮.০৮ g·mol−১ | ||
| বর্ণ | Colourless liquid | ||
| গন্ধ | Pungent, irritating, floral, cucumber like | ||
| ঘনত্ব | 0.7845 g/cm3 (25 °C) | ||
| গলনাঙ্ক | −৯৪.৭ °সে (−১৩৮.৫ °ফা; ১৭৮.৫ K)[8] | ||
| স্ফুটনাঙ্ক | ৫৬.০৫ °সে (১৩২.৮৯ °ফা; ৩২৯.২০ K)[8] | ||
পানিতে দ্রাব্যতা |
Miscible | ||
| দ্রাব্যতা | Miscible in benzene, diethyl ether, methanol, chloroform, ethanol[9] | ||
| লগ পি | −0.16[10] | ||
| বাষ্প চাপ |
| ||
| অম্লতা (pKa) | |||
চৌম্বকক্ষেত্রের প্রতি সংবেদনশীলতা (χ) |
−33.78·10−6 cm3/mol | ||
| প্রতিসরাঙ্ক (nD) | 1.3588 (VD = 54.46) | ||
| সান্দ্রতা | 0.295 mPa·s (25 °C)[9] | ||
| গঠন | |||
| Coordination geometry |
Trigonal planar at C2 | ||
| আণবিক আকৃতি | Dihedral at C2 | ||
| ডায়াপল মুহূর্ত | 2.91 D | ||
| তাপ রসায়নবিদ্যা | |||
| তাপ ধারকত্ব, C | 125.45 J/(mol·K) | ||
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
200.4 J/(mol·K) | ||
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
(−250.03) – (−248.77) kJ/mol | ||
| দহনে প্রমান এনথ্যাল্পির পরিবর্তন ΔcH |
−1.772 MJ/mol | ||
| ঝুঁকি প্রবণতা | |||
| জিএইচএস চিত্রলিপি |   | ||
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক | ||
| জিএইচএস বিপত্তি বিবৃতি | H225, H319, H336, H373 | ||
| জিএইচএস সতর্কতামূলক বিবৃতি | P210, P235, P260, P305+351+338 | ||
| এনএফপিএ ৭০৪ | 
১
৩ | ||
| ফ্ল্যাশ পয়েন্ট | −২০ °সে (−৪ °ফা; ২৫৩ K) | ||
অটোইগনিশন তাপমাত্রা |
৪৬৫ °সে (৮৬৯ °ফা; ৭৩৮ K) | ||
| বিস্ফোরক সীমা | 2.6–12.8%[13] | ||
| Threshold Limit Value | 1185 mg/m3 (TWA), 2375 mg/m3 (STEL) | ||
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |||
LD৫০ (মধ্যমা ডোজ) |
| ||
LC৫০ (মধ্যমা একাগ্রতা) |
20,702 ppm (rat, 8 h)[14] | ||
LCLo (সর্বনিম্ন প্রকাশিত) |
45,455 ppm (mouse, 1 h)[14] | ||
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |||
PEL (অনুমোদনযোগ্য) |
1000 ppm (2400 mg/m3)[7] | ||
REL (সুপারিশকৃত) |
TWA 250 ppm (590 mg/m3)[7] | ||
IDLH (তাৎক্ষণিক বিপদ |
2500 ppm[7] | ||
| সম্পর্কিত যৌগ | |||
সম্পর্কিত যৌগ |
| ||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
অ্যাসিটোন পানিতে সম্পূর্ণভাবে মিশে যায় এবং গুরুত্বপূর্ণ জৈব দ্রাবক বিবেচিত হয়। ২০১০ সালে ৬.৭ মিলিয়ন টন অ্যাসিটোন উৎপন্ন হয়েছিল। দ্রাবক হিসেবে ব্যবহার ছাড়াও মিথাইল মেথিক্রিলেট ও বিসফেনল এ তৈরিতেও অ্যাসিটোন ব্যবহার করা হয়। [16] নেইলপলিশ দূরীকারক এবং তুলি পাতলাকারকেও অ্যাসিটোনের ব্যবহার বিদ্যমান।
স্বাভাবিক বিপাকীয় প্রক্রিয়ায় মানবদেহেও অ্যাসিটোন উৎপন্ন হয়। রক্ত ও মূত্রে এটি অধিক পরিমাণে উপস্থিত। বহুমূত্র রোগীদের দেহ বিপুল পরিমাণে অ্যাসিটোন তৈরি করে থাকে। প্রজননসংক্রান্ত সমস্যার ক্ষেত্রে এটি খুব বেশি অসুবিধাজনক বিবেচিত হয় না। শিশুদের মৃগীরোগ প্রতিকারেও অ্যাসিটোন ব্যবহার করা হয়। [17]