From Wikipedia, the free encyclopedia
Es denomina espectre de l'hidrogen a l'espectre d'emissió electromagnètica pròpia de l'hidrogen. Les longituds d'ona venen determinades per la fórmula de Rydberg. Aquestes línies espectrals observades són degudes als electrons que es mouen entre nivells energètics de l'àtom. Les línies espectrals són importants en astronomia per poder detectar la presència d'hidrogen i per poder calcular els desplaçaments cap al roig.
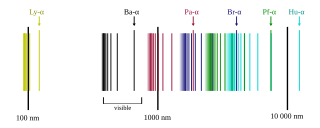
Les diferències d'energia entre nivells del model de Bohr –i, per tant, les longituds d'ona dels fotons emesos i absorbits– venen donades per la fórmula de Rydberg:[1]
On n és el nivell d'energia inicial, n′ és el nivell d'energia final i R és la constant de Rydberg.[2] Els valors significatius només s'obtenen quan n és major que n′ i es pren el límit d'u entre infinit com zero.
Totes les longituds d'ona es donen amb fins a 3 xifres significatives.
| n | λ (nm) |
|---|---|
| 2 | 121,6 |
| 3 | 102,6 |
| 4 | 97,3 |
| 5 | 95,0 |
| 6 | 93,8 |
| 91,2 |

Aquesta sèrie s'anomena en honor del seu descobridor, Theodore Lyman. Totes les longituds d'ona de la sèrie de Lyman estan a la banda ultraviolada.[3][4]
| n | λ (nm) |
|---|---|
| 3 | 656 |
| 4 | 486 |
| 5 | 434 |
| 6 | 410 |
| 7 | 397 |
| 365 | |

| n | λ (nm) |
|---|---|
| 4 | 1870 |
| 5 | 1280 |
| 6 | 1090 |
| 7 | 1005 |
| 8 | 954 |
| 820 |
Les línies de Pasched cauen totes a la banda infraroja.[5]
| n | λ (nm) |
|---|---|
| 5 | 4050 |
| 6 | 2620 |
| 7 | 2160 |
| 8 | 1940 |
| 9 | 1820 |
| 1460 |
| n | λ (nm) |
|---|---|
| 6 | 7460 |
| 7 | 4650 |
| 8 | 3740 |
| 9 | 3300 |
| 10 | 3040 |
| 2280 |
| n | λ (nm) |
|---|---|
| 7 | 12400 |
| 8 | 7500 |
| 9 | 5910 |
| 10 | 5130 |
| 11 | 4670 |
| 3280 |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.