Relativní atomová hmotnost
From Wikipedia, the free encyclopedia
Remove ads
Relativní atomová hmotnost (též poměrná atomová hmotnost) je podíl klidové hmotnosti atomu a atomové hmotnostní konstanty. Pro jeden atom přibližně odpovídá nukleonovému číslu, tj. počtu nukleonů v jádře. U prvků v přírodě je dána poměrným zastoupením izotopů prvku.
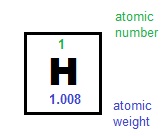
Značení
- Symbol veličiny: Ar
- Jednotka: bezrozměrná veličina
Měření
K měření relativní atomové hmotnosti se používá hmotnostní spektrometr (hmotnostní spektrometrie).
Výpočet
Relativní atomová hmotnost je určena vztahem
kde ma je klidová hmotnost atomu a mu je atomová hmotnostní konstanta (1,661×10−27 kg).
Vlastnosti
Relativní atomová hmotnost je rovna číselné hodnotě atomové hmotnosti vyjádřené v (unifikovaných) atomových hmotnostních jednotkách (značka u), též zvaných dalton (značka Da).
Číselně je relativní atomová hmotnost rovna molární hmotnosti vyjádřené v gramech na mol.
Relativní atomová hmotnost pro některé prvky
V následující tabulce jsou uvedeny relativní atomové hmotnosti některých prvků za předpokladu přirozeného zastoupení izotopů. Pro srovnání je uveden izotop s největším zastoupením (v závorce je uveden jeho molární zlomek); lze vidět, že relativní atomová hmotnost je blízká jeho nukleonovému číslu, což souvisí s definicí atomové hmotnostní konstanty:
kde hmotnost neutronu je pouze o 0.14 % větší než hmotnost protonu.
Remove ads
Související články
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads



 ...
...