χημική ένωση From Wikipedia, the free encyclopedia
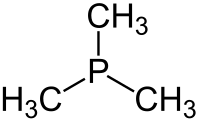
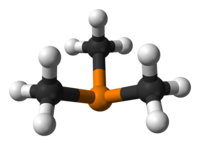
Η τριμεθυλοφωσφίνη[1] (αγγλικά: trimethylphosphine) είναι οργανική χημική ένωση, που περιέχει άνθρακα, υδρογόνο και φωσφόρο, με χημικό τύπο C3H9P. Eίναι η απλούστερη τριτοταγής (δηλαδή τριυποκατεστημένη) οργανική φωσφίνη. Είναι το φωσφορούχο ανάλογο της τριμεθυλαμίνης. Μπορεί να θεωρηθεί ότι προέρχεται από τη «μητρική» ένωση «φωσφίνη» (PH3), με αντικατάσταση όλων [δηλαδή και των τριών (3)] ατόμων υδρογόνου της τελευταίας από τρία (3) μεθύλια (CH3-). Η χημικά καθαρή τριμεθυλαμίνη, στις συνηθισμένες συνθήκες, δηλαδή σε θερμοκρασία 25 °C και υπό πίεση 1 atm, είναι άχρωμο πυροφορικό (δηλαδή που αυτοαναφλέγεται εύκολα) και τοξικό υγρό. Με επίδρσση υποχλωριώδους νατρίου (NaClO) μπορεί να μετατραπεί σε μη πυροφορικό τριμεθυλοφωσφινοξείδιο [(CH3)3PO)]. Με βάση το χημικό τύπο της (C3H9P) έχει τρία (3) ισομερή θέσης:
| Τριμεθυλοφωσφίνη | |||
|---|---|---|---|
 | |||
 | |||
| Γενικά | |||
| Όνομα IUPAC | Τριμεθυλοφωσφίνη | ||
| Άλλες ονομασίες | Τριμεθυλοφωσφαμίνη Τριμεθυλοφωσφίνη Τριμεθυλοφωσφάνιο μεθυλο-2-φωσφαπροπάνιο | ||
| Χημικά αναγνωριστικά | |||
| Χημικός τύπος | C2H7P | ||
| Μοριακή μάζα | 76,07 | ||
| Σύντομος συντακτικός τύπος | (CH3)3P | ||
| Συντομογραφίες | Me3P | ||
| Αριθμός CAS | 594-09-2 | ||
| SMILES | CP(C)C | ||
| Δομή | |||
| Διπολική ροπή | 1,19 D | ||
| Είδος δεσμού | σ (2sp3-3sp3, C-P) | ||
| Πόλωση δεσμού | 3% (C--P+) | ||
| Γωνία δεσμού | 118° (CPC) | ||
| Μοριακή γεωμετρία | τριγωνική πυραμιδική | ||
| Ισομέρεια | |||
| Ισομερή θέσης | 3 Προπανοφωσφαμίνη-1 Προπανοφωσφαμίνη-2 P-μεθυλαιθανοφωσφαμίνη | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | -86 °C | ||
| Σημείο βρασμού | 38-39 °C | ||
| Πυκνότητα | 735 kg/m3 | ||
| Διαλυτότητα στο νερό | μικρή | ||
| Εμφάνιση | άχρωμο πυροφορικό υγρό | ||
| Χημικές ιδιότητες | |||
| Επικινδυνότητα | |||
| Φράσεις κινδύνου | 11-36/37/38 | ||
| Φράσεις ασφαλείας | 9-16-26-36/37/39 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Με επίδραση μεθυλομαγνησιοβρωμίδιου (CH3MgBr) σε τριχλωριούχο φωσφόρο (PCl3) παράγεται τριμεθυλοφωσφίνη[2]:
Με επίδραση διμεθυλοφωσφίνης (CH3PHCH3) σε μεθυλαλογονίδιο (CH3X) παράγεται τριμεθυλοφωσφίνη[3][4]:
Η τριμεθυλοφωσφίνη έχει έντονο πυρηνόφιλο χαρακτήρα, λόγω της μεγάλης επιδεκτικότητας πόλωσης του φωσφόρου[4].
Η αντίδραση με αλκυλαλογονίδια παράγεται τεταρτοταγές αλογονούχο αλκυλοτριμεθυλοφωσφώνιο {[RP(CH3)3]X}[3][4]:
Γενικά, οι ενώσεις του τρισθενούς φωσφόρου, μπορούν να χρησιμοποιηθούν ως αναγωγικά μέσα, για να αφαιρέσουν οξυγόνο ή θείο από διάφορες ενώσεις. Μερικά σχετικά παραδείγματα είναι τα ακόλουθα[3][4]:
1. Αναγωγή θειοξειδίων (RSOR) σε θειαιθέρες (RSR):
2. Αναγωγή νιτρωδοαλκανίων (RNO) σε αμίνες (RNH2)
3. Αναγωγή οξιράνιου σε αιθένιο:
4. Αναγωγή θειιράνιου σε αιθένιο:
Με επίδραση μεθυλενίου ([:CH2]) σε τριμεθυλοφωσφίνη παράγεται αιθυλοδιμεθυλοφωσφίνη[5]:
Η τριμεθυλοφωσφίνη παράγει επίσης ένα μεγάλο αριθμό ενώσεων συναρμογής, συμπεριφερόμενη ως βάση κατά Lewis, με διάφορα μέταλλα. Π.χ. αντιδρά με τον πεντακαρβονυλοσίδηρο [Fe(CO)5], σχηματίζοντας τετρακαρβονυλοτριμεθυλοφωσφινοσίδηρο [Fe(CO)4P(CH3)3]:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.