Plumba (II) nitrato aŭ nitrato de plumbo (II) estas neorganika kombinaĵo apartenanta al la familio de la saloj, rezultanta el interagado de la nitrata acido kaj plumba (II) hidroksido. Plumba (II) nitrato estas blanka solidaĵo, solvebla en akvo, alkoholoj kaj aliaj nepolaraj organikaj solvantoj. Plumba (II) nitrato prezentas plumbatomon ligitan al nitrataj grupoj per jonaj ligiloj. Ĝi konsistas je 1 plumbatomoj, 2 nitrogenatomoj, 6 oksigenatomoj kaj uzatas en kemiaj sintezoj.
| Plumba (II) nitrato | ||||||
| Kemia formulo | ||||||
 | ||||||
| Alternativa(j) nomo(j) | ||||||
| ||||||
| CAS-numero-kodo | 10099-74-8 | |||||
| ChemSpider kodo | 23300 | |||||
| PubChem-kodo | 24924 | |||||
| Fizikaj proprecoj | ||||||
| Aspekto | blanka solidaĵo[1] | |||||
| Molmaso | 331,208g mol−1 | |||||
| Denseco | 4,53 g/cm−3 | |||||
| Fandpunkto | 83°C [2] | |||||
| Bolpunkto | 470°C [3][4] | |||||
| Refrakta indico | 1,7820 | |||||
| Ekflama temperaturo | Nebrulema | |||||
| Solvebleco | Akvo:343 g/L | |||||
| Mortiga dozo (LD50) | 270 mg/kg (buŝe) | |||||
| GHS etikedigo de kemiaĵoj | ||||||
| GHS Damaĝo Piktogramo |
| |||||
| GHS Signalvorto | Damaĝa substanco | |||||
| GHS Deklaroj pri damaĝoj | H272, H302, H317, H318, H332, H351, H360, H372, H373, H400, H410 | |||||
| GHS Deklaroj pri antaŭgardoj | P203, P210, P220, P260, P261, P264, P264+265, P270, P271, P272, P273, P280, P301+317, P302+352, P304+340, P305+354+338, P317, P318, P319, P321, P330, P333+313, P362+364, P370+378, P391, P405, P501 | |||||
(25 °C kaj 100 kPa) | ||||||
Historio
Plumba (II) nitrato unue estis identigita en 1597 fare de la alkemiisto Andreas Libavius, kiu nomis la substancon plumbum dulce, kun la signifo "dolĉa plumbo", pro ĝia gusto. Ĝi estas produktata komerce per reago de metala plumbo kun densa nitrata acido en kiu ĝi estas malmulte solvebla. Ĝi estis produktata kiel krudmaterialo por farado de pigmentoj kiel ekzemple kroma-flavaĵo (plumba (II) kromiato, PbCrO4), kromia-oranĝo (baza plumba (II) kromiato, Pb2CrO5) kaj Napola flavaĵo. Tiuj pigmentoj estis uzitaj por tinkturado kaj presado de kalikoto kaj aliaj teksaĵoj. Ĝi estis uzata kiel oksidigaĵo en la nigra pulvoro kaj kune kun plumbazido en specialaj eksplodaĵoj.
Reakcio 1
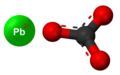
- Reakcio de plumba (II) karbonato kun nitrata acido donante plumban nitraton:[5]
Reakcio 2
- Preparado de plumba nitrato per traktado de nitrata acido kun plumba hidroksido:
Reakcio 3
- Preparado de plumba nitrato per traktado de nitrata acido kun plumba (II) oksido:
Reakcio 4
- Preparado de plumba (II) sulfato per traktado de natria sulfato kun plumba (II) nitrato:
Reakcio 5
- Reakcio de plumba (II) nitrato kun kalia jodido donante plumban (II) jodidon
Vidu ankaŭ
Referencoj
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.






![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)