
Ácido bórico
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Ácido bórico?
Resumir este artículo para un niño de 10 años
El ácido bórico o ácido trioxobórico(III) es un compuesto químico, ligeramente ácido. Es usado como antiséptico, insecticida, retardante de la llama, espumante y precursor de otros compuestos químicos. Es usado también como agente tampón para regulación del pH.
 | ||
 | ||
| Nombre IUPAC | ||
| Ácido trioxobórico(III) | ||
| General | ||
| Otros nombres |
Borato(III) de hidrógeno Ácido ortobórico | |
| Fórmula semidesarrollada | B(OH)3 | |
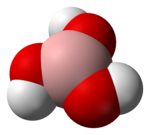
| Fórmula estructural | Véase imagen | |
| Fórmula molecular | H3BO3 | |
| Identificadores | ||
| Número CAS | 10043-35-3[1] | |
| ChEBI | 33118 | |
| ChEMBL | CHEMBL42403 | |
| ChemSpider | 7346 | |
| DrugBank | 11326 | |
| PubChem | 7628 | |
| UNII | R57ZHV85D4 | |
| KEGG | C12486 D01089, C12486 | |
| Propiedades físicas | ||
| Apariencia | Blanco cristalino | |
| Densidad | 1435 kg/m³; 1,435 g/cm³ | |
| Masa molar | 6183 g/mol | |
| Punto de fusión | 442 K (169 °C) | |
| Punto de ebullición | 573 K (300 °C) | |
| Propiedades químicas | ||
| Acidez | 1=9,236; 2=12,74; 3=13,80 pKa | |
| Propiedades farmacológicas | ||
| Categoría embarazo | Puede perjudicar a la fertilidad. Puede dañar al feto | |
| Termoquímica | ||
| ΔfH0gas | -992.28 kJ/mol | |
| ΔfH0sólido | -1093.99 kJ/mol | |
| S0gas, 1 bar | 295.23 J·mol–1·K | |
| S0sólido | 88,7 J·mol–1·K–1 | |
| Peligrosidad | ||
| SGA |
 | |
| NFPA 704 |
0
1
0
| |
| Frases H | H360FD | |
| Frases P |
P201 P280 | |
| Riesgos | ||
| Riesgos principales | Puede perjudicar a la fertilidad. Puede dañar al feto. | |
| Ingestión | Tóxico. Vómitos y diarrea en pequeñas dosis; en dosis mayores puede ser letal. | |
| Inhalación | Puede causar irritación. | |
| Piel | Puede causar irritación. | |
| Ojos | Puede causar irritación. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Hasta 1981 se usaba como ingrediente en abonos foliares y en la conservación de alimentos como el marisco, aunque a partir de 1983, por recomendación de las administraciones, se fue sustituyendo por el metabisulfito sódico y, en la actualidad, su uso es ilegal.
Existe en forma cristalina (polvo de cristales blancos) que se disuelve fácilmente en agua. Su fórmula química es H3BO3. La forma mineral de este compuesto se denomina sassolita. Comúnmente se utiliza para realizar baños pédicos.

