
Lämmastikhape
keemiline ühend / From Wikipedia, the free encyclopedia
Lämmastikhape (varem: salpeeterhape; keemiline valem HNO3) on söövitav värvuseta teravalõhnaline vedelik ja mürgine hape, mis võib põhjustada raskeid põletushaavu. Lämmastikhape on laialt levinud hapetest üks tugevamaid happeid.
| Lämmastikhape | |
|---|---|
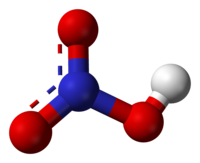 Lämmastikhappe molekuli mudel | |
| Üldised omadused | |
| Keemiline valem | HNO3 |
| Välimus | värvuseta või pruun vedelik |
| Füüsikalised omadused | |
| Molekuli mass | 63,0 amü |
| Sulamistemperatuur | 231,15 K (−42 °C) |
| Keemistemperatuur | 356,15 K (83 °C) |
| Tihedus | 1,522×10³ kg/m³ |
| Lahustuvus | segunev |
| Termokeemia | |
| ΔfH0gaas | –134,31 kJ/mol |
| ΔfH0vedel | –174 kJ/mol |
| ΔfH0tahke | –184 kJ/mol |
| S0gaas | 266,39 J/mol·K |
| S0vedel | 156 J/mol·K |
| Ohutus | |
| Suukaudne manustamine | võib kahjustada seedeelundeid |
| Nahk | võib põhjustada raskeid söövitushaavu, arme, plekke jms |
| Silmad | võib kahjustada nägemist |
| Kasutatakse SI-süsteemi ühikuid. Kui pole teisiti öeldud, eeldatakse normaaltingimusi. | |
Lämmastikhappel on iseloomulik terav lämmatav lõhn, mis pisut meenutab kloori lõhna. Toatemperatuuril eraldub kontsentreeritud, veevabast lämmastikhappest lämmastikdioksiidist koosnevat punast või kollast gaasi.
Kontsentreeritud lämmastikhapet nimetatakse lenduvaks lämmastikhappeks. Kuna see sisaldab lahustunud lämmastikdioksiidi, on see punakat (kollakat, pruunikat) värvi. Lämmastikhape on väga tugev oksüdeerija, mis võib orgaanilisi, kergsüttivaid aineid süüdata.
Lämmastikhape on lämmastiku hapnikhapetest kõige tuntum ja kõige püsivam, mis kuulub mineraalhapete ja üheprootoniliste hapete hulka.
Lämmastikhapet sisaldub ka happevihmades.