Acide fluorosulfurique
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Acide fluorosulfurique?
Résumez cet article pour un enfant de 10 ans
L'acide fluorosulfurique, également appelé acide fluorosulfonique, est un composé chimique de formule HSO3F. C'est un liquide peu visqueux, soluble dans les solvants polaires tels que le nitrobenzène, l'acide acétique et l'acétate d'éthyle, mais peu soluble dans les solvants apolaires tels que les alcanes. Il s'agit d'un superacide de pKa égal à -10 dont le mélange équimolaire avec le pentafluorure d'antimoine SbF5 donne l'acide magique HSO3F·SbF5, un acide parmi les plus forts connus. Cette acidité lui permet de dissoudre pratiquement n'importe quelle substance organique, même les composés faiblement accepteurs de protons.
| Acide fluorosulfurique | |
 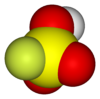 Structure de l'acide fluorosulfurique. |
|
| Identification | |
|---|---|
| Nom UICPA | acide fluorosulfurique |
| Synonymes |
acide fluorosulfonique |
| No CAS | 7789-21-1 |
| No ECHA | 100.029.227 |
| No CE | 232-149-4 |
| No RTECS | LP0715000 |
| PubChem | 24603 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore |
| Propriétés chimiques | |
| Formule | HFO3SHSO3F ou HFSO3 |
| Masse molaire[1] | 100,07 ± 0,006 g/mol H 1,01 %, F 18,99 %, O 47,96 %, S 32,04 %, |
| pKa | -10 |
| Propriétés physiques | |
| T° fusion | −87,3 °C |
| T° ébullition | 165,5 °C |
| Solubilité | Soluble dans l'eau |
| Masse volumique | 1,84 (liquide) |
| Précautions | |
| SGH[2] | |
| H314 et H332 H314 : Provoque de graves brûlures de la peau et des lésions oculaires H332 : Nocif par inhalation |
|
| SIMDUT[3] | |
  E, F, E : Matière corrosive Transport des marchandises dangereuses : classe 8 F : Matière dangereusement réactive réagit violemment au contact de l'eau en dégageant un gaz très toxique : chlorure d'hydrogène Divulgation à 1,0% selon la liste de divulgation des ingrédients |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
HSO3F s'hydrolyse lentement en acide fluorhydrique et acide sulfurique ; l'acide triflique HSO3CF3, qui lui est structurellement apparenté, est plus stable dans l'eau.

