
Sulfure de zinc
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Sulfure de zinc?
Résumez cet article pour un enfant de 10 ans
Le sulfure de zinc désigne principalement deux corps ioniques inorganiques dimorphes, également composés de cations zinc et d'anions sulfures en proportion stoechiométrique, de formule ZnS. Le chimiste et le minéralogiste distinguent nettement le sulfure de zinc alpha ZnS α, de structure hexagonale, légèrement moins dense, correspondant à la wurtzite encore improprement dénommée blende hexagonale, et le sulfure de zinc bêta ZnS β, de structure cristalline cubique, correspondant à la sphalérite ou à l'ancienne blende minérale si commune dans la nature. Il existe également ZnS γ, de structure tétragonale très rare, de couleur noire à grise, nommée polhémusite, de formule (Zn, Hg)S.
| Sulfure de zinc | |
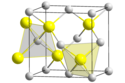 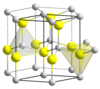 Sphalérite (blende) et wurtzite, les deux formes cristallines du sulfure de zinc. |
|
| Identification | |
|---|---|
| Nom UICPA | sulfure de zinc(II) |
| No CAS | 1314-98-3 |
| No ECHA | 100.013.866 |
| No CE | 215-251-3 |
| No RTECS | ZH5400000 |
| PubChem | 14821 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche à beige, inodore |
| Propriétés chimiques | |
| Formule | SZnZnS |
| Masse molaire[1] | 97,45 ± 0,03 g/mol S 32,91 %, Zn 67,11 %, |
| Propriétés physiques | |
| T° fusion | 1 700 °C[2], soluble dans les acides minéraux, insoluble dans l'acide acétique |
| T° ébullition | 1 180 °C (sublimation)[3] |
| Solubilité | presque insoluble dans l'eau[3] |
| Masse volumique | 4,1 g·cm-3[4] |
| Propriétés électroniques | |
| Bande interdite | 3,54 eV (cubique, 300 K)[réf. souhaitée] 3,91 eV (hexagonal, 300 K)[réf. souhaitée] |
| Cristallographie | |
| Système cristallin | cubique (sphalérite) hexagonal (wurtzite) |
| Précautions | |
| SGH[3] | |
| n'est pas une substance dangereuse pour le SGH | |
| NFPA 704 | |
| Transport[3] | |
non-soumis à régulation |
|
| Écotoxicologie | |
| DL50 | 2 000 mg/kg (rat, oral)[5] 2 000 mg/kg (rat, dermique)[5] |
| CL50 | 5,04 mg/l (rat, inhalation, 4 h)[5] 1 830 mg/l (poissons, 96 h)[6],[7] 0,97 mg/l (crustacés, 48 h)[7] |
| Composés apparentés | |
| Autres cations | Sulfure de cadmium Sulfure de mercure(II) |
| Autres anions | Oxyde de zinc, Séléniure de zinc Tellurure de zinc |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Si la couleur des minéraux peut être foncée voire noire à cause de la présence d'impuretés variées, ces corps purs dimorphes, très solubles dans les acides minéraux, sont blancs à légèrement colorés. Sous une forme dense, le sulfure de zinc synthétique ZnS β d'indice de réfraction 2,368 peut être transparent et être utilisé comme fenêtre en optique visible et infrarouge.
