
Tiosulfato
composto químico / From Wikipedia, the free encyclopedia
O tiosulfato (S
2O2−
3) é un oxianión de xofre.
| Tiosulfato | |
|---|---|
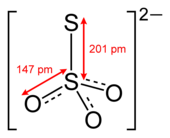 | |
 | |
sulfurotioato | |
| Identificadores | |
| Número CAS | 14383-50-7 |
| PubChem | 1084 |
| ChemSpider | 1054 |
| ChEBI | CHEBI:16094 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | S 2O2− 3 |
| Masa molecular | 112,13 g·mol−1 |
| Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O prefixo tio- indica que o ión tiosulfato é un ión sulfato cun dos seus átomos de oxíxeno substituído por xofre. O tiosulfato ten unha forma molecular tetraédrica con simetría C3v. O tiosulfato aparece de forma natural e prodúcese ou utilízase en certos procesos bioquímicos. Serve para desclorar rapidamente a auga e é notable polo seu uso para deter o branqueamento na industria papeleira. Tamén é útil para fundir a mena de prata, na produción de artigos de coiro, e para estabilizar tinguiduras en produtos téxtiles.
O tiosulfato de sodio, comunmente chamado hipo (de "hiposulfito"), foi amplamente utilizado en fotografía para fixar os negativos en branco e negro e as impresións despois da etapa de revelado; os fixadores modernos 'rápidos' usan como sal fixador o tiosulfato de amonio porque actúa tres ou catro veces máis rápido.[2]
Algunhas bacterias poden metabolizar os tiosulfatos; por exemplo pode utilizarse como doante de electróns na fotosíntese anoxixénica, e a maioría das bacterias redutoras de sulfato poden reducir tamén o tiosulfato; igualmente, as arqueas Pyrolobus poden usalo como aceptor de electróns.[3]