
フェンタニル
鎮痛剤として用いられる強力な合成オピオイド / ウィキペディア フリーな encyclopedia
親愛なるWikiwand AI, これらの重要な質問に答えるだけで、簡潔にしましょう:
トップの事実と統計を挙げていただけますか フェンタニル?
この記事を 10 歳向けに要約してください
すべての質問を表示
フェンタニル (Fentanyl) は、鎮痛剤として使用される非常に強力な合成オピオイドである。ほかの薬物とともに、麻酔[1]、集中治療室での鎮痛、鎮静[2]に用い、術後鎮痛や癌性疼痛の鎮痛にも適応がある[3]。
概要 IUPAC命名法による物質名, 臨床データ ...
 | |
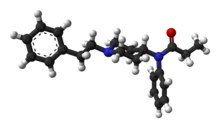 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 発音 | /ˈfɛntənɪl/ or /ˈfɛntənəl/ |
| 販売名 | フェンタニル[4]、フェントス[5]、イーフェン[6]、アブストラル(Abstral)[7]、デュロテップ[8]、ワンデュロ[9]、Sublimaze[10]、Instanyl[11]、Lazanda[12] |
| Drugs.com | monograph |
| MedlinePlus | a605043 |
| ライセンス | EMA:リンク、US Daily Med:リンク |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 依存性 | 高い[13] |
| 投与経路 | 口腔粘膜、硬膜外麻酔、筋肉内注射、髄腔内(英語版)、静脈注射、舌下(英語版)、経皮吸収パッチ |
| 薬物動態データ | |
| 生物学的利用能 | 92% (経皮) 89% (鼻腔) [14] 50% (頬粘膜) 33% (消化管) 100% (筋肉注射) 80% (吸入) 100% (静脈注射) |
| 血漿タンパク結合 | 80–85%[15] |
| 代謝 | 肝臓、主としてCYP3A4による。 |
| 作用発現 | 5分[16] |
| 半減期 | IV: 6分 (T1/2 α) 1時間 (T1/2 β) 16時間(T1/2 ɣ) 鼻腔内: 15-25時間[17] 経皮: 20–27時間[17] 舌下 (単回): 5–13.5時間[17] 頬粘膜: 3.2-6.4時間[17] |
| 作用持続時間 | IV: 30–60 minutes[16][18] |
| 排泄 | 主に尿から代謝物が排泄 ( 10%以上は未変化体として)[17] |
| 識別 | |
| CAS番号 |
437-38-7 |
| ATCコード | N01AH01 (WHO) N02AB03 (WHO) |
| PubChem | CID: 3345 |
| IUPHAR/BPS | 1626 |
| DrugBank |
DB00813 |
| ChemSpider |
3228 |
| UNII |
UF599785JZ |
| KEGG |
D00320 |
| ChEBI |
CHEBI:119915 |
| ChEMBL |
CHEMBL596 |
| PDB ligand ID | 7V7 (PDBe, RCSB PDB) |
| 化学的データ | |
| 化学式 | C22H28N2O |
| 分子量 | 336.48 g·mol−1 |
| |
| 物理的データ | |
| 密度 | 1.1 g/cm3 |
| 融点 | 87.5 °C (189.5 °F) |
| テンプレートを表示 | |
閉じる