トップQs
タイムライン
チャット
視点
ハロゲン化アルカリ金属
ウィキペディアから
Remove ads
ハロゲン化アルカリ金属(Alkali metal halide)は、Mをアルカリ金属、Xをハロゲンとして、化学式MXで表される無機化合物である。しばしばこれらの金属やハロゲンの重要な供給源となる。最も有名なものは、食卓塩として使われる塩化ナトリウムである[1]。

構造
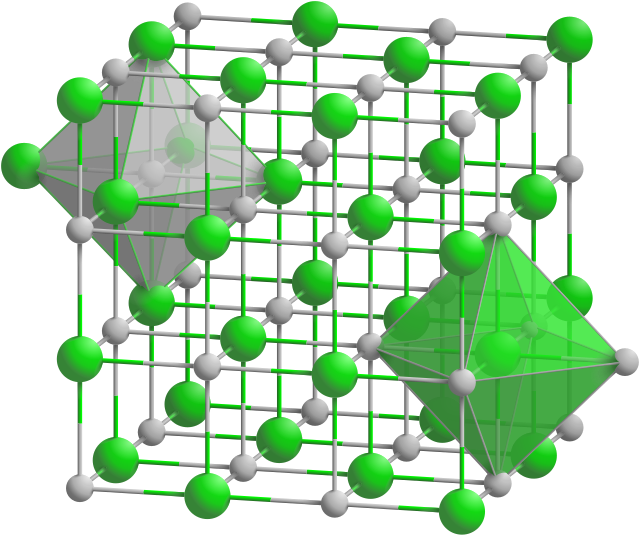
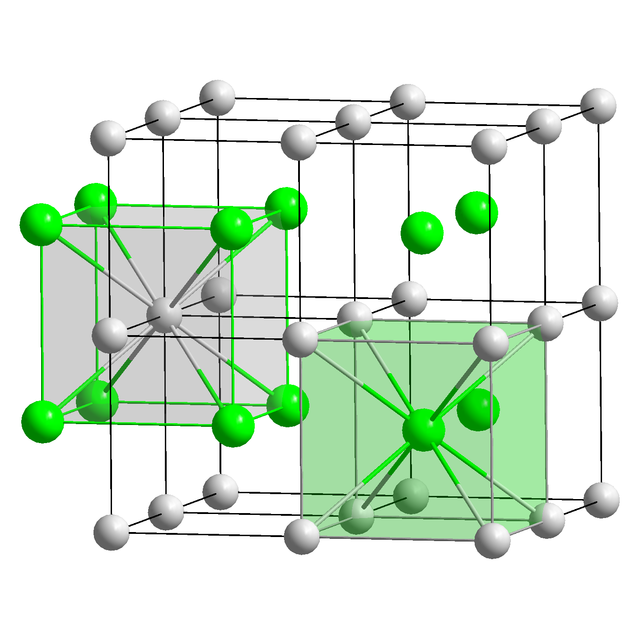
大部分のハロゲン化アルカリ金属は、面心立方格子状に結晶化する。この構造では、金属もハロゲンも八面体の配置となり、各々のイオンの配位数は6となる。塩化セシウム、臭化セシウム、ヨウ化セシウムは体心立方格子状に結晶化し、より大きな金属カチオン(アニオンも同様)に関して、配位数は8となる[2]。
性質
ハロゲン化アルカリ金属は、無色の結晶質固体であるが、細かいものは白色を呈する。高温で溶融し、通常数百℃で無色の液体になる。その高い融点は、格子エネルギーの高さを反映している。静かで高い温度では、これらの液体は二原子分子の気体を作る。
これらの化合物は極性溶媒に溶解し、溶媒和しやすいアニオン及びカチオンを含むイオン溶液となる。アルカリ金属は、対応するアルカリ金属をかなりの量、溶かす。セシウムは融点以上の全ての温度で、完全に混和性である[3]。
下の表は、各々の化合物の記事へのリンクを与えている。化合物名の横の数字は、ポーリングのスケールに基づく元素間の電気陰性度の差を示している。数字が大きいほど、固体がよりイオン性であることを表す。
Remove ads
出典
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
