
კალიუმის ჰიდროქსიდი
From Wikipedia, the free encyclopedia
კალიუმის ჰიდროქსიდი — ქიმიური ნივთიერება ფორმულით KOH. არის თეთრი ფერის, არაგამჭვირვალე, მყარი, კრისტალური, წყალში კარგად ხსნადი ტუტე ლითონის ჰიდროქსიდი. წყალში გახსნისას გამოჰყოფს დიდი რაოდენობით სითბოს. წყალხსნარებში ის მთლიანად დისოცირდება და წარმოადგენს ძლიერ ტუტეს. ამჟღავნებს ფუძის ყველა თვისებას, ჰაერზე შთანთქავს ტენსა და ნახშირბადის დიოქსიდს, ამის გამო კომერციული ნიმუშების უმეტესობა არის დაახლოებით, 90% სისუფთავის, დანარჩენი ნივთიერებები წყალი და კარბონატებია. მოლეკულაში ჟანგბადი ერთი ბმით უკავშირდება წყალბადს, ხოლო მეორეთი კალიუმის ატომს.[7] კალიუმის ჰიდროქსიდი ურთიერთქმედებს ინდიკატრებთან, იისფერ ლაკმუსს ალურჯებს, ხოლი უფერო ფენოლფთალეინს ჟოლოსფრერ შეფერილობას აძლევს.
სწრაფი ფაქტები ზოგადი, ფიზიკური თვისებები ...
| კალიუმის ჰიდროქსიდი | |
 | |
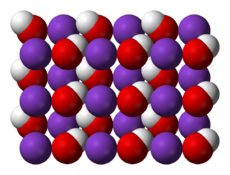 | |
| ზოგადი | |
|---|---|
| სისტემური სახელწოდება | კალიუმის ჰიდროქსიდი |
| ტრადიციული სახელწოდება | კაუსტიკური პოტაში კალიუმის ჰიდრატი |
| ქიმიური ფორმულა | KOH |
| მოლური მასა | 56.11 გ/მოლი |
| ფიზიკური თვისებები | |
| სიმკვრივე | 2.044 (20 °C-ზე) გ/სმ³[1] 2.12 (25 °C-ზე)[2][3] გ/სმ³ |
| თერმული თვისებები | |
| დნობის ტემპერატურა | 360[4] °C |
| დუღილის ტემპერატურა | 1327 [3] °C |
| წარმოქმნის ენტალპია (სტ. პირ.) | -425.8[2][5] კჯ/მოლი |
| ქიმიური თვისებები | |
| pKa | −0.7[6] |
დახურვა