
하이포플루오로산
From Wikipedia, the free encyclopedia
하이포플루오로산(Hypofluorous acid) 또는 차아불소산은 화학식이 HOF인 화합물이다. 플루오린에 의하여 물이 산화되면서 만들어진 중간 생산물이며 플루오린화 수소와 산소를 만들어낸다. 고체로 분리가 가능한 산이다. 하이포플루오로산은 매우 폭발적이게 산소와 HF로 분해되는 경향이 있다.[1] 얼음을 플루오로화시켜 순수한 형태로 분리시킨다.
간략 정보 이름, 식별자 ...
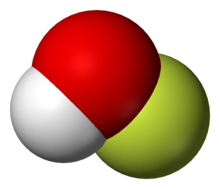
 Gas-phase structure | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름
Hypofluorous acid | |
| 별칭
Hydrogen hypofluorite Hydrogen fluorate(-I) Fluoric(-I) acid Hydrogen monofluoroxygenate(0) hydroxyl fluoride | |
| 식별자 | |
3D 모델 (JSmol) |
|
| ChemSpider |
|
PubChem CID |
|
CompTox Dashboard (EPA) |
|
| |
| |
| 성질 | |
| HOF | |
| 몰 질량 | 36.0057 g mol−1 |
| 겉보기 | pale yellow liquid above −117 °C white solid below −117 °C |
| 녹는점 | −117 °C (−179 °F; 156 K) |
| 끓는점 | decomposes at 0 °C 틀:Reference needed |
| 구조 | |
점군 |
Cs |
| 위험 | |
| 주요 위험 | strong oxidizer, corrosive |
| NFPA 704 (파이어 다이아몬드) | |
| 관련 화합물 | |
다른 양이온 |
lithium hypofluorite |
관련 화합물 |
hypochlorous acid nitroxyl hydrogen cyanide formaldehyde |
닫기
고체 상태에서 화합물의 구조는 엑스선결정학을 통해 분석할 수 있으며,[1] 분자의 결합각은 101°이다. O-F 결합과 O-H결합은 각각 144.2, 96.4 피코미터이고, 고체상태에서는 O–H···O형태의 연결을 통해 사슬모양을 유지한다. 가스의 상태에서는 H-O-F 결합각은 97.2°로 고체일때보다 약간 더 작다.
플루오린의 산소산중 하나이다. 영하 40℃에서 얼음에 F2기체를 노출시킴으로써 얻어진 기체상태의 HOF를 농축하여 얻어낸다.
- F2 + H2O → HOF + HF
상온에서는 매우 폭발적으로 플루오린화 수소와 산소 기체로 분리된다.
- 2 HOF → 2 HF + O2
아세토나이트릴속의 하이포플루오로산("젖은" 아세토나이트릴위로 기체상태의 플루오린을 노출시켜 생성할 수 있다.)은 친전자적인 산소 전달 물질이며,[2][3] 이를 페난트롤린과 반응시키면 1,10-phenanthroline dioxide를 내놓게된다.[4][5]
모든 구성 원자가 다르기 때문에 대칭 구조를 찾기 힘들다. 항등원 E와 세 원자를 지나는 거울형 대칭에 의해서만 대칭이다. 이러한 구조를 가지는 분자 집단을 Cs로 지칭한다.
