
Ideālas gāzes likums
From Wikipedia, the free encyclopedia
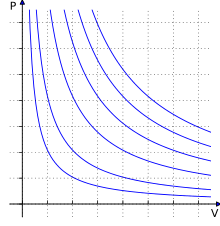
Ideālas gāzes likums ir hipotētiskās ideālās gāzes stāvokļa vienādojums. To var izmantot arī reālām gāzēm zemā spiedienā un augstā temperatūrā, lai noteiktu sakarību starp temperatūru, spiedienu un tilpumu. Tas ir Boila—Mariota, Šarla un Gē-Lisaka likumu apvienojums ar Avogadro likumu.
Pirmais to izteica francūzis Benuā Klapeirons (Benoît Émile Clapeyron) 1834. gadā.[1] 1874. gadā krievs Dmitrijs Mendeļejevs likumā ieviesa universālo gāzu konstanti R, tā aizvietojot lielo daudzumu specifisko gāzu konstanšu.[2][3][4]