
Gp120
De Wikipedia, a enciclopédia encyclopedia
A glicoproteína do envelope GP120 é uma glicoproteína exposta na superfície do envelope do HIV. Foi descoberta pelos Professores Tun-Hou Lee e Myron "Max" Essex da Harvard School of Public Health em 1988. O 120 em seu nome vem de seu peso molecular de 120 kDa. O Gp120 é essencial para a entrada de vírus nas células, pois desempenha um papel vital no apego a receptores de superfície celular específicos. Estes receptores são DC-SIGN, Heparan Sulfate Proteoglycan e uma interação específica com o receptor CD4, particularmente nas células T. A ligação ao CD4 induz o início de uma cascata de mudanças conformacionais em gp120 e gp41 que levam à fusão da membrana viral com a membrana da célula hospedeira. A ligação ao CD4 é principalmente eletrostática, embora haja interações van der Waals e ligações de hidrogênio.
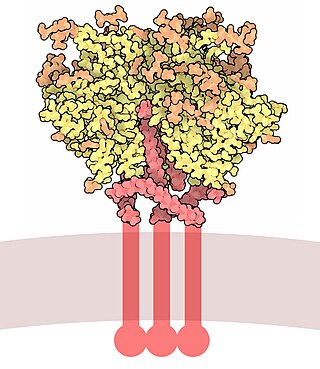
O Gp120 é codificado pelo gene HIV, que tem cerca de 2,5 kb de comprimento e códigos para cerca de 850 aminoácidos. O produto primário do env é a proteína gp160, que é clivada para gp120 (~480 aminoácidos) e gp41 (~345 aminoácidos) no retículo endoplasmático pela protease celular furina. A estrutura cristalina do núcleo do gp120 mostra uma organização com um domínio externo, um domínio interno com respeito a sua terminologia e uma folha de ponte. Gp120 é ancorado à membrana viral, ou envelope, através de ligações não covalentes com a glicoproteína transmembrana, gp41. Três gp120s e gp41s se combinam em um trimer de heterodímeros para formar o espigão do envelope, o que medeia a fixação e a entrada na célula hospedeira.