Top Qs
Linha do tempo
Chat
Contexto
Fórmula de Rydberg
Da Wikipédia, a enciclopédia livre
Remove ads
A fórmula de Rydberg (fórmula de Rydberg-Ritz) ou equação de Rydberg é utilizada em física atômica para determinar todo o espectro da luz emitida pelo hidrogênio, posteriormente estendida para uso com qualquer elemento pelo uso do princípio de combinação de Rydberg-Ritz.[1][2]
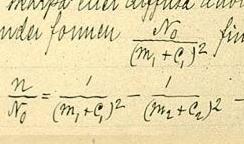
O espectro é o conjunto de comprimentos de onda dos fótons emitidos quando o elétron pula entre níveis de energia discretos, "camadas" ao redor do átomo de um certo elemento químico. A descoberta posteriormente promoveu motivação para a criação da física quântica.[3]
A fórmula foi inventada pelo físico sueco Johannes Rydberg e apresentada em 5 de Novembro de 1888.
Remove ads
Fórmula de Rydberg para o hidrogênio
Resumir
Perspectiva
Onde
- é o comprimento de onda da luz emitida no vácuo,[1]
- é a constante de Rydberg para o hidrogênio,[4]
- and são inteiros tais que .
Deixando igual a 1 e fazendo percorrer de 2 até o infinito, as linhas de espectro conhecidas como série de Lyman convergem em 91 nm. Da mesma maneira:
| Nome | Converge para | ||
| 1 | Série de Lyman | 91 nm | |
| 2 | Série de Balmer | 365 nm | |
| 3 | Série de Paschen | 821 nm | |
| 4 | Série de Brackett | 1459 nm | |
| 5 | Série de Pfund | 2280 nm | |
| 6 | Série de Humphreys | 3283 nm |
Apenas a série de Balmer está na faixa visível do espectro luminoso. A série de Lyman está na faixa ultravioleta, e as séries de Paschen, Brackett, Pfund, e Humphreys, na infravermelha.
Remove ads
Fórmula de Rydberg para qualquer elemento semelhante ao hidrogênio
Resumir
Perspectiva
A fórmula acima pode ser estendida para qualquer elemento químico semelhante ao hidrogênio.[1][4]
onde
- é o comprimento de onda da luz emitida no vácuo;
- é a constante de Rydberg para esse elemento;
- é o número atômico;
- e são inteiros tais que .
É importante notar que esta fórmula pode ser aplicada apenas para elementos semelhantes ao hidrogênio, também chamados átomos hidrogênicos ou hidrogenóides, isto é,.átomos com apenas um elétron na orbital mais externo. Exemplos destes incluem o etc.[5]
Remove ads
Ver também
- Princípio de combinação de Rydberg-Ritz
- Johannes Rydberg
- constante de Rydberg
- Átomo de Bohr
- Espectro do átomo de hidrogênio
Referências
- Martinson, Indrek; L.J. Curtis (2005). «Janne Rydberg – his life and work» (PDF). NIM B. 235: 17–22. doi:10.1016/j.nimb.2005.03.137 (em inglês)
- Jastrow, Robert (1948). «On the Rydberg-Ritz Formula in Quantum Mechanics». Phys. Rev. 73. 60 páginas. doi:10.1103/PhysRev.73.60 (em inglês)
Remove ads
Bibliografia
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads