From Wikipedia, the free encyclopedia
Cistin je dimerna aminokiselina formirana oksidacijom dva ostatka cisteina koja su kovalentno vezana disulfidnom vezom. Ovo organosumporno jedinjenje ima formulu (SCH2CH(NH2)CO2H)2. Cistin je beli prah, koji se topi na 247-249 °C. Otkrio ga je 1810 Vilijam Hid Volaston. Tek je 1899. bilo pokazano da se cistin može dobiti iz proteina. Te godine je bio izolovan iz goveđih rogova.[4] Putem formiranja disulfidnih veza unutar i između molekula proteina, cistin je značajan determinant tercijarne strukture većine proteina. Na primer, disulfidno vezivanje, zajedno sa vodoničnim vezama i hidrofobnim interakcijama, je parcijalno odgovorno za formiranje glutenske osnove hleba. Ljudska kosa sadrži aproksimativno 5% cistina po masi.[5]
| Cistin | |
|---|---|
 |
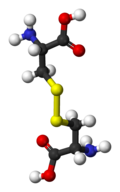 |
| Identifikacija | |
| CAS registarski broj | 56-89-3 |
| ChemSpider[1] | 575 |
| UNII | 48TCX9A1VT |
| KEGG[2] | |
| ChEMBL[3] | CHEMBL366563 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | C6H12N2O4S2 |
| Molarna masa | 240.3 g mol−1 |
| Opasnost | |
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS |
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |
| Infobox references | |
Disulfidna veza se lako redukuje i daje korespondirajući tiol cistein. Ova reakcija je tipično ostvaruje sa tiolima kao što su merkaptoetanol ili ditiotreitol.
Iz tog razloga, nutriciona korist i izvori cistina su identični sa cisteinom. Disulfidne veze se otvaraju brže na višim temperaturama.[6].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.