From Wikipedia, the free encyclopedia
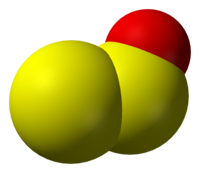
இருகந்தக ஓராக்சைடு (Disulfur monoxide or sulfur suboxide) என்பது S2O என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மம் ஆகும். இச்சேர்மம் டைசல்பர் மோனாக்சைடு, கந்தக கீழாக்சைடு என்ற பெயர்களாலும் அழைக்கப்படுகிறது. கீழ்நிலை கந்தக ஆக்சைடுகளில் ஒன்றான இது நிறமற்ற ஒரு வாயுவாகும். வாயு நிலையிலிருந்து ஒடுக்கமடையும் போது, அறை வெப்பநிலையில் நிலைப்புத்தன்மையற்ற வெளிர் நிற திண்மமாக இவ்வாயு மாறுகிறது[3] . S-S-O பிணைப்புக் கோணம் 117.88° , S-S பிணைப்பு நீளம் 188.4 பைக்கோ மீட்டர், S-O பிணைப்பு நீளம் 146.5 பைக்கோ மீட்டர் என்ற அளவுகள் கொண்ட ஒரு வளைவு மூலக்கூறாக இதன் கட்டமைப்பு உள்ளது[4]
 | |
 | |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
கந்தக கீழாக்சைடு; கந்தகவாக்சைடு; | |
| இனங்காட்டிகள் | |
| 20901-21-7 [1] | |
| ChemSpider | 124163 |
InChI | |
| பண்புகள் | |
| S2O | |
| வாய்ப்பாட்டு எடை | 80.1294 கி/மோல்[1] |
| தோற்றம் | நிறமற்ற வாயு அல்லது அடர் சிவப்பு திண்மம்[2] |
| கட்டமைப்பு | |
| ஒருங்கிணைவு வடிவியல் |
வளைவு |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | நச்சு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
இருகந்தக ஓராக்சைடை பல்வேறு வழிகளில் தயாரிக்க இயலும். கந்தகத்தை குறைவான அளவு ஆக்சிசனில் எரியவைத்து இருகந்தக ஓராக்சைடு தயாரிக்கலாம். கந்தகத்தை தாமிர ஆக்சைடுடன் சேர்த்து ஆக்சிசனேற்றம் செய்வதன் மூலமும் இதைத் தயாரிக்கலாம்:[5]
தயோனைல் குளோரைடுடன் வெள்ளி சல்பைடு சேர்த்து வினைபுரியச் செய்வதன் மூலமாகவும் இதைத் தயாரிக்க முடியும்.:
கந்தக டை ஆக்சைடை ஒளிர்விறக்கத்தில் வெப்பச்சிதைவுக்கு உட்படுத்துவதன் மூலமாகவும் இதைத் தயாரிக்க முடியும். கார்பன் நாற்குளோரைடில் மஞ்சள் நிறக் கரைசலாக இருகந்தக ஓராக்சைடு உருவாகிறது[5]. திரவ நைட்ரசன் வெப்பநிலையில் திடப்பொருளாக இதைப் பெறவியலும். பெரும்பாலும் மாசுக்கள் கலந்து அடர்த்தியான நிறத்தில் காணப்படும். அறை வெப்பநிலையில் இருகந்தக ஓராக்சைடு சிதைவடைந்து பலகந்தக ஆக்சைடுகள் தோன்றுவதன் வழியாக கந்தக டை ஆக்சைடாக இது உருவாகிறது[6]
கந்தக ஆவி மற்றும் கந்தக டை ஆக்சைடு வாயு ஆகியனவற்றை ஒளிர்விறக்கம் செய்து 1933 ஆம் ஆண்டில் பீட்டர் டபிள்யூ செங்கு இருகந்தக ஓராக்சைடைக் கண்டறிந்தார்[7] இவ்வாயுவை அவர் கண்டறிந்த பொழுது, சில மணி நேரங்கள் மட்டுமே நிலைத்து இருக்கும் தன்மையும் தூய கண்ணாடியில் ஒற்றை இலக்க அளவு பாதரச அழுத்தமும் கொண்ட வாயுவாகவே அறிந்தார். சிதைவடையும் பொழுது இவ்வாயு கிட்டத்தட்ட 30 மி.மீ பாதரச அழுத்தத்தை வெளிப்படுத்தியதால் செங்கு இவ்வாயுவின் மூலக்கூற்று வாய்ப்பாட்டை SO என நிர்ணயம் செய்து கந்தக ஓராக்சைடு எனப் பெயரிட்டார். 1940 ஆம் ஆண்டில் கே.கொந்திராட் இவா மற்றும் வி. கொந்திராட் இவ் இருவரும் இவ்வாயுவின் மூலக்கூற்று வாய்ப்பாட்டை S2O2 என நிர்ணயம் செய்து இருகந்தக ஈராக்சைடு என்ற பெயரைப் பரிந்துரை செய்தனர். 1956 ஆம் ஆண்டில் ஆர்.யே. மையர்சு மற்றும் டி.யே.மெச்சி ஆகியோர் இவ்வாயுவை ஆய்வு செய்தனர். சரியான பகுதிப்பொருட்களும் S2O என்ற மூலக்கூறு வடிவமைப்பும் உறுதி செய்யப்பட்டன[8] .
டிசல்ஃபோவைப்ரியோ வகை பாக்டிரியாக்கள் இருகந்தக ஓராக்சைடை உற்பத்தி செய்வதாக அறியப்படுகிறது[9] S<su. பெரும்பாலும் இவ்வாயு ஐ.ஓ (சந்திரன்) எரிமலையில் இருந்து வருவதாக நம்பப்படுகிறது[10] . கந்தகம் மற்றும் கந்தக டை ஆக்சைடு வாயுக்கள் எரிமலையில் இருந்து வெளிப்படும்பொழுது அதிக வெப்பத்திலும் 100 பார் அழுத்தத்திலும் 1 முதல் 6 % வாயு உருவாவதாக கூறப்படுகிறது. ஐ.ஓ (சந்திரன்) மீதுள்ள பீலெ எரிமலை திடநிலையில் இருக்கும் இருகந்தக ஓராக்சைடால் சூழப்பட்டுள்ளதாக நம்பப்படுகிறது.
செறிவான S2O திண்மம் 420 மற்றும் 530 நானோமீட்டர்களில் உட்கவர் பட்டைகளை காட்சிப்படுத்துகிறது. சேர்மத்தில் S3 மற்றும் S4 அமைப்புகளின் இருப்பு இதற்கான காரணமாகும்[11] . S2O இன் நுண்ணலை அலைக்கற்றையானது ஏ=41915.44, பி=5059.07, மற்றும் C=4507.19 மெகா எர்ட்சு என்ற சுழல் வரைகூறுகளைப் பெற்றுள்ளது.[12]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.