அமோனியம் நைட்ரேட்டு
NH<sub>4</sub>NO<sub>3 </sub> என்ற மூலக்கூறு வாய்ப்பாடு கொண்ட ஒரு வேதிச் சேர்மம் From Wikipedia, the free encyclopedia
Remove ads
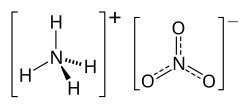
அம்மோனியம் நைட்ரேட்டு (Ammonium nitrate) என்பது அம்மோனியம் நேர்மின் அயனியின் நைட்ரேட் உப்பாகிய ஒரு வேதிச்சேர்மம் ஆகும். இதனுடைய வேதி வாய்ப்பாடு NH4NO3, எளிமையாக N2H4O3. இது ஒரு வெண்மை நிறப்படிகத் திண்மம் ஆகும். நீரில் அதிகம் கரையும் தன்மை கொண்டது. இது மிக முக்கியமாக விவசாயத்துறையில் அதிக அளவில் நைட்ரஜனைத் தரக்கூடிய உரமாகப் பயன்படுகிறது.[4] இந்தச் சேர்மமானது சுரங்கத்தொழில் மற்றும் கட்டுமானத் துறையில் பயன்படுத்தப்படும் வெடிபொருட்களின் ஒரு முக்கியப் பகுதிப்பொருளாகவும் திகழ்கிறது. வட அமெரிக்காவில் அதிகமாகப் பயன்படுத்தப்படும் ஒரு பிரபலமான தொழில் துறை வெடிபொருளான ANFO என்பதன் பகுதிப்பொருளாக இருக்கிறது. இந்தச் சேர்மமானது தவறாகப் பயன்படுத்தப்படும் வாய்ப்புகள் அதிகமாக இருப்பதால், பல நாடுகளில், இச்சேர்மத்தைப் பொதுவான நுகர்வோர் பயன்படுத்துவதற்கு, கட்டுப்பாடுகள் விதிக்கப்பட்டுள்ளன.
Remove ads
கிடைக்கும் தன்மை
சிலி நாட்டிலுள்ள அடகாமா பாலைவனத்தின் மிகவும் வறட்சியான பகுதிகளில் அம்மோனியம் நைட்ரேட்டானது, (அம்மோனியா நைட்ர் - சால்ட்பீட்டர் எனப்படும் அம்மோனியத்தை ஒத்த பொருளாகவும், சோடியம் நைட்ரேட் எனப்படும் நைட்ரேட் சோ்மமாகவும்) இயற்கையான கனிமமாகக் கிடைக்கிறது. கடந்த காலத்தில், அம்மோனியம் நைட்ரேட்டானது, சுரங்கத் தொழிலின் மூலமாகப் பெறப்பட்டது. நடைமுறையில் தற்போது பயன்படுத்தப்படும் அம்மோனியம் நைட்ரேட்டானது 100 % தொகுப்பு முறையில் தயாரிக்கப்பட்டதாகும்.
Remove ads
தயாரிப்பு
- அம்மோனியம் நைட்ரேட்டின் தொழில் முறை தயாரிப்பானது, அமில கார வினையின் அடிப்படையிலானது. இவ்வினையில், அம்மோனியாவானது, நைட்ரிக் அமிலத்துடன் வினைப்பட்டு அம்மோனியம் நைட்ரேட்டானது கிடைக்கிறது.[5]
- NH3 + HNO3 → NH4NO3
- நீரற்ற வாயு நிலையில் உள்ள அம்மோனியாவும், அடர் நைட்ரிக் அமிலமும் இவ்வினையில் பயன்படுத்தப்படுகின்றன. இந்த வினையானது, அதிக அளவிலான வெப்ப உமிழ் வினையாக இருக்கும் காரணத்தால், தீவிரமான வினையாக உள்ளது. 83% செறிவுள்ள கரைசலாக உருவான பிறகு, மிகுதியாக உள்ள நீரானது ஆவியாக்கப்பட்டு 95% முதல் 99.9% வரை செறிவுள்ள அம்மோனியம் நைட்ரேட் கிடைக்கப்பெறுகிறது. இவ்வாறு கிடைக்கும் அம்மோனியம் நைட்ரேட் உருக்கானது, சிறு மணிகளாக தூவி கோபுரம் மூலமாக உருவாக்கப்படுகின்றன. இந்த அம்மோனியம் நைட்ரேட் மணிகள் அல்லது குருணைகள் கெட்டிப்படுவதைத் தடுக்க, மேலும் உலர்த்தப்பட்டு, குளிர்விக்கப்படுகின்றன. இவ்வாறு கிடைக்கக்கூடிய குறுமணிகள், வணிகரீதியான அம்மோனியம் நைட்ரேட் இறுதி விளைபொருளாகும்.
- இந்த வினைக்கான அம்மோனியாவானது, ஹேபர் முறையில் நைட்ரஜனையும் ஹைட்ரஜனையும் இணைப்பதன் மூலம் கிடைக்கிறது. ஹேபர் முறையில் தயாரிக்கப்ட்ட அம்மோனியாவானது, ஆஸ்ட்வால்ட் முறையில் நைட்ரிக் அமிலமாக, ஆக்சிஜனேற்ற வினையின் மூலம் மாற்றப்படுகிறது.
- மற்றுமொரு தயாரிப்பு முறையானது, ஒட்டா முறை :
- Ca(NO3)2 + 2NH3 + CO2 + H2O → 2NH4NO3 + CaCO3
விளைபொருட்களான கால்சியம் கார்பனேட் மற்றும் அம்மோனியம் நைட்ரேட் ஆகியவை தனித்தனியாக, துாய்மைப்படுத்தப்பட்டோ அல்லது கால்சியம் அம்மோனியம் நைட்ரேட்டாக மாற்றப்பட்டோ விற்பனை செய்யப்படலாம்.
- அம்மோனியம் நைட்ரேட் மெட்டாதெஸிஸ் வினை மூலமாகவும் பெறப்படலாம்.:
- (NH4)2SO4 + Ba(NO3)2 → 2 NH4NO3 + BaSO4
- NH4Cl + AgNO3 → NH4NO3 + AgCl
வேதி வினைகள்
- அம்மோனியம் நைட்ரேட், உலோக ஐதராக்சைடுகளுடன் வினைப்பட்டு, கார உலோக நைட்ரேட்டுகளை உருவாக்குவதுடன், அம்மோனியாவையும் வெளியிடுகிறது.
- NH4NO3 + MOH → NH3 + H2O + MNO3 (M= Na, K)
- அம்மோனியம் நைட்ரேட் வெப்பப்படுத்தும் போது, மீதப்பொருட்களை அல்லது எச்சத்தை விட்டுச் செல்வதில்லை.
- NH4NO3 → N2O + 2H2O
- அம்மோனியம் நைட்ரேட்டானது வளிமண்டலத்தில் NO, SO2, மற்றும் NH3 மற்றும் இரண்டாம் நிலை பகுதிப்பொருளான PM10 உமிழ்தலால் உருவாக்கப்படுகிறது[6]
படிக நிலைகள்
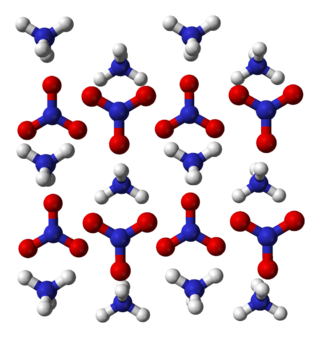
- வெப்பநிலை மற்றும் அழுத்தத்தில் ஏற்படும் மாறுபாடு காரணமாக படிக நிலைகளில் ஏற்படும் மாறுபாடுகள் அம்மோனியம் நைட்ரேட்டின் இயற்பியல் பண்புகளில் பாதிப்பை ஏற்படுத்துகின்றன. மூன்று படிக நிலைகள் அறியப்பட்டவையாக உள்ளன.
- ஐந்தாவது அமைவான படிகமானது, சீசியம் குளோரைடைப் போன்று போலி கனசதுர அமைப்பைக் கொண்டுள்ளது. நைட்ரேட் எதிர்மின் அயனி மற்றும் அம்மோனியம் நேர்மின் அயனியின் நைட்ரஜன் அணுக்கள், கன சதுர வரிசையில் சீசியம் குளோரைடு படிகத்தில் சீசியம் மற்றும் குளோரின் அணுக்கள் ஆக்கிரமித்த இடங்களை ஆக்கிரமித்துக் கொள்கின்றன.[7]
Remove ads
பயன்பாடுகள்
உரங்கள்
NPK விகித முறைப்படி 34-0-0 (34% nitrogen) அம்மோனியம் நைட்ரேட்டானது ஒரு மிக முக்கியமான உரமாகும்.[8] இது சற்றே யூரியாவை (46-0-0) விட செறிவு குறைந்ததாக இருப்பதால் சரக்கை கையாள்வதில் ஒரு சிறிய குறையைக் கொண்டுள்ளது. அம்மோனியம் நைட்ரேட்டானது யூரியாவை விட நிலைப்புத் தன்மை கொண்டது. இது எளிதில் வளிமண்டலத்தில் நைட்ரஜனை இழப்பதில்லை. மழையை எதிர்பார்த்திருக்கும் நேரத்தில் முந்தைய மிதமான வெப்பத்தில் யூரியாவை பயன்படுத்துவது நைட்ரஜன் இழப்பைத் தவிர்ப்பதற்கான வழியாகும்.[9][10]
வெடிபொருட்கள்
அம்மோனியம் நைட்ரேட்டானது தனித்த நிலையில் வெடிக்கக்கூடிய தன்மை உடையதல்ல.[11] ஆனால் இது முதன்மையான வெடிபொருட்களான அசைடுகள், அல்லது எரிபொருட்களான அலுமினியத்துாள் அல்லது எரிபொருள் எண்ணெய் ஆகியவற்றுடன் சேர்க்கும் போது வெவ்வேறு விதமான பண்புகளை உடைய வெடிபொருட்களை வெகு விரைவாக உருவாக்குகின்றது.
பாதுகாப்பு நடவடிக்கைகள்
வழங்குநர்களிடமிருந்து கிடைக்கும் பாதுகாப்பு தரவுத் தாள்களில் சுகாதாரம் மற்றும் பாதுகாப்புத் தொடர்பான தகவல்கள் இணையம் மற்றும் இணையத்தளத்தில் காணக் கிடைக்கின்றன. பல வெடிவிபத்துகளில் எண்ணற்ற மக்கள் உயிரிழந்ததைத் தொடர்ந்து அமெரிக்க சுற்றுச்சூழல் பாதுகாப்பு நிறுவனம், தொழில்சார் உடல்நலம் மற்றும் பாதுகாப்பு நிறுவனம் மற்றும் ஆல்ககால், புகையிலை மற்றும் துப்பாக்கி அடுக்கமைப்பு நிறுவனம் ஆகியவவை இணைந்து கூட்டாக பாதுகாப்பு வழிகாட்டுதல்களை வழங்கின. வெப்பம் அல்லது எந்தவிதமான தீப்பற்றும் பற்றவைப்பு ஆதாரமும் தீவிரமான எரிதலுக்கும் அல்லது வெடிப்புக்கும் காரணமாக இருக்கலாம்.
அம்மோனியம் நைட்ரேட்டு ஓரு திடமான ஆக்சிசனேற்றியாக இருப்பதால் எரியும் பொருட்கள் மற்றும் ஒடுக்கமடையும் பொருட்களுடன் நன்றாக வினைபுரிகிறது. இருப்பினும் அது முக்கியமாக உரமாகவும் வெடிபொருளாகவும் பயன்படுத்தப்படுகிறது. குளங்கள் தோண்டுவதற்காக சில நேரங்களில் பூமியை வெடிக்கச் செய்யவும் இது பயன்படுத்தப்படுகிறது. அம்மோனியம் நைட்ரேட்டு அமடோல் வடிவத்தில் டிரைநைட்ரோதொலுயீன் போன்ற மற்ற வெடிப்பொருட்களின் வெடிப்பு வீதத்தை மாற்ற பயன்படுகிறது.
அம்மோனியம் நைட்ரேட்டை சேமிப்பதற்கும் பராமரிப்பதற்கும் பல பாதுகாப்பு வழிமுறைகள் கொடுக்கப்பட்டுள்ளன. தீப்பற்றும் பொருட்களுக்கு அருகில் இதைச் சேமிக்கக்கூடாது. குளோரேட்டுகள், கனிம அமிலங்கள் மற்றும் உலோக சல்பைடுகள் போன்ற சில வேதிப் பொருட்களுடன் சேர்த்து வைக்க அம்மோனியம் நைட்ரேட்டு பொருத்தமற்றது, இதனால் தீவிரமான அல்லது வன்முறை சிதைவுகள் உண்டாகும்.
அம்மோனியம் நைட்ரேட் 59.4% என்ற அளவில் ஈரப்பதம் கொண்டிருக்கிறது, இது வளிமண்டலத்தில் இருந்து ஈரப்பதத்தை உறிஞ்சிவிடும். எனவே, இறுக்கமாக மூடப்பட்ட கொள்கலனில் அம்மோனியம் நைட்ரேட்டை சேமிப்பது முக்கியம். இல்லையெனில் அது ஒரு பெரிய திடமான பொருளாக ஒன்று திரண்டுவிடும்.
அம்மோனியம் நைட்ரேட்டு போதுமான அளவு ஈரப்பதத்தை உறிஞ்சிக் கொண்டு நீர்மமாக மாறிவிடும். வேறு சில உரங்களுடன் அம்மோனியம் நைட்ரேட்டை கலந்தால் ஒப்பீட்டளவு ஈரப்பதம் குறைகிறது.
அமோனியம் நைட்ரேட்டை வெடிப்பொருளாக பயன்படுத்துவதற்கான சாத்தியம் இருப்பதால் ஒழுங்குமுறை நடவடிக்கைகளை தொடங்கின. உதாரணமாக, ஆத்திரேலியாவில் ஆபத்தான பொருட்கள் ஒழுங்குமுறை விதிகள் ஆகத்து 2005 ஆம் ஆண்டு முதல் நடைமுறைக்கு வந்தது. இத்தகைய ஆபத்தான பொருட்களை கையாள்வதற்கு உரிமம் பெறுதல் நடைமுறைக்கு வந்தது. தவறான பயன்பாட்டைத் தடுப்பதற்கான , பொருத்தமான பாதுகாப்பு நடவடிக்கைகள் ஏற்படுத்தப்பட்டன. இவ்விதிகளைப் பின்பற்றும் விண்ணப்பதாரர்களுக்கு மட்டுமே உரிமம் வழங்கப்பட்டது.
கல்வி மற்றும் ஆராய்ச்சி நோக்கங்கள் போன்ற நடவடிக்கைகள் கருத்தில் கொள்ளப்பட்டன. ஆனால் தனிப்பட்ட நபர்கள் பயன்பாட்டுக்கு அனுமதி மறுக்கப்பட்டது.
உரிமங்களைக் பெற்றுக் கொண்ட ஊழியர்களும் அங்கீகரிக்கப்பட்ட நபர்கள் மூலம் மேற்பார்வை செய்யப்பட வேண்டும் என்று சட்டம் இயற்றப்பட்டது. மேலும், அவர்களுக்கு உரிமம் வழங்கப்படுவதற்கு முன்னர் காவல் துறையினரின் அனுமதி பெற வேண்டும் என்றும் விதி வகுக்கப்பட்டிருந்தது.
Remove ads
உடல் நலம்
வழங்குநர்களிடமிருந்து கிடைக்கும் பாதுகாப்பு தரவுத் தாள்களில் சுகாதாரம் மற்றும் பாதுகாப்புத் தொடர்பான தகவல்கள் இணையம் மற்றும் இணையத்தளத்தில் தொடர்ச்சியாக வெளியிடப்படுகிறது.
அமோனியம் நைட்ரேட்டு உடல் நலத்திற்கு எத்தகைய கேட்டையும் விளைவிக்காது என்பதால் உரமாகப் பயன்படுத்தப்படுகிறது. இதனுடைய உயிர் கொல்லும் அளவு 2,217 மி.கி./கி.கி. ஆகும். இது மேசை உப்பின் உயிர் கொல்லும் அளவில் மூன்றில் இரண்டு பங்கு மட்டுமேயாகும்.
Remove ads
பேரழிவுகள்
அம்மோனியம் நைட்ரேட்டை சூடுபடுத்தும் போது, அது நைட்ரசு ஆக்சைடு மற்றும் நீராவியாகச் சிதைவடைகிறது. இது ஒரு வெடிக்கும் வினை அல்ல என்றாலும், திடீர் வெடிப்பு மூலம் வெடித்துச் சிதற, தூண்டப்படலாம். அமோனியம் நைட்ரேட்டின் அதிக அளவு கையிருப்பு, ஆக்சிசனேற்றத்தின் காரணமாக, ஒரு பெரிய தீ விபத்தாக முடியலாம். 1947 ஆம் ஆண்டு டெக்சாசு நகரத்தில் இத்தகைய ஒரு பேரழிவு நடந்தது. இதனால் அமோனியம் நைட்ரேட்டை சேமிப்பது மற்றும் கையாளுதலுக்கான கட்டுப்பாடுகளில் முக்கிய மாற்றங்கள் ஏற்பட்டன.
Remove ads
மேற்கோள்கள்
புற இணைப்புகள்
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads