Топ питань
Часова шкала
Чат
Перспективи
Карбонатна кислота
хімічна сполука З Вікіпедії, вільної енциклопедії
Remove ads
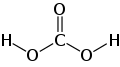
Карбона́тна кислота́, також ву́гільна, вуглецева кислота́ (вуглекислота) — слабка двоосновна кислота з хімічною формулою H2CO3. У чистому вигляді нестійка[1]. Утворюється в малих кількостях при розчиненні вуглекислого газу у воді, в тому числі і вуглекислого газу з повітря. Утворює ряд стійких неорганічних та органічних похідних: солі (карбонати та гідрокарбонати), естери, аміди та ін
Remove ads
Фізичні властивості
Молекула вугільної кислоти має плоску будову. Центральний вуглецевий атом має sp²-гібридизацію. У гідрокарбонат- карбонат-аніонів відбувається делокалізація π-зв'язку. Довжина зв'язку C—O в карбонат-іоні становить 129 пм.
Хімічні властивості
Узагальнити
Перспектива
Рівновага у водних розчинах та кислотність
Вугільна кислота існує у водних розчинах в стані рівноваги з гідратом діоксиду вуглецю:
- , константа рівноваги при 25 °C
Швидкість прямої реакції 0,039 с−1, зворотної — 23 с−1.
У свою чергу розчинений гідрат діоксиду вуглецю знаходиться в рівновазі з газоподібним діоксидом вуглецю:
- ]
Дана рівновагу при підвищенні температури зсувається вправо, а при підвищенні тиску — вліво (докладніше див. Абсорбція газів).
Вугільна кислота піддається оборотньому гідролізу, створюючи при цьому кисле середовище:
- , константа кислотної дисоціації при 25 °C
Однак, для практичних розрахунків частіше використовують уявну константу кислотності, що враховує рівновагу вугільної кислоти з гідратом діоксиду вуглецю:
гідрокарбонат-іон піддається подальшому гідролізу по реакції
- , константа кислотності при 25 °C
Таким чином, в розчинах, що містять вугільну кислоту, створюється складна рівноважна система, яку можна зобразити у загальному вигляді таким чином:
Значення pH в такій системі, яке відповідає насиченому розчину діоксиду вуглецю в воді при 25 °C і тиску 760 мм рт. ст., можна розрахувати по формулі:
- , где L = 0,034 моль/л — розчинність CO2 в воді при вказаних умовах.
Розкладання
При збовтуванні, підвищенні температури розчину і/або пониженні парціального тиску діоксиду вуглецю рівновагу в системі зміщується вліво, що призводить до розкладання частини вугільної кислоти на воду і діоксид вуглецю. При кипінні розчину вугільна кислота розкладається повністю:
Взаємодія з основами та солями
Вугільна кислота вступає в реакції нейтралізації з розчинами основ, утворюючи середні та кислі солі (хімія) — карбонати та гідрокарбонати відповідно:
- (конц.) ]
- (розч.) ]
- ]
- ]
При взаємодії вугільної кислоти з карбонатами утворюються гідрокарбонати:
Remove ads
Отримання
Узагальнити
Перспектива
Вугільна кислота утворюється при розчиненні у воді діоксиду вуглецю:
Вміст вугільної кислоти в розчині збільшується при зниженні температури розчину та збільшенні тиску вуглекислого газу.
Також вугільна кислота утворюється при взаємодії її солей (карбонатів та гідрокарбонатів) з більш сильною кислотою. При цьому велика частина утворилася вугільної кислоти, як правило, розкладається на воду і діоксид вуглецю:
Remove ads
Застосування
Вугільна кислота завжди присутня у водних розчинах вуглекислого газу (див. Газована вода).
В біохімії використовується властивість рівноважної системи змінювати тиск газу пропорційно зміні змісту іонів оксонію (кислотності) при постійній температурі. Це дозволяє реєструвати в реальному часі хід ферментативних реакцій, що протікають із зміною pH розчину.
Органічні похідні
Вугільну кислоту формально можна розглядати як карбонову кислоту з гідроксильною групою замість вуглеводневої залишку. У цій якості вона може утворювати всі похідні, характерні для карбонових кислот[2].
Деякі представники подібних сполук перераховані в таблиці.
Remove ads
Див. також
Примітки
Література
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads



![{\displaystyle K_{p}=\ {\frac {\ \mathrm {[H_{2}CO_{3}]} }{\ \mathrm {[CO_{2}\ \cdot H_{2}O]} }}=1,70\ \cdot 10^{-3}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/5ef6f8727b849294458faf393c418c372521c01f)


![{\displaystyle K_{a1}=\ {\frac {\ \mathrm {[HCO_{3}^{-}]\ \cdot [H_{3}O^{+}]} }{\ \mathrm {[H_{2}CO_{3}]} }}=2,5\ \cdot 10^{-4}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/6950909768e276a9790eade365511107494b0390)
![{\displaystyle K_{a}'=\ {\frac {\ \mathrm {[HCO_{3}^{-}]\ \cdot [H_{3}O^{+}]} }{\ \mathrm {[CO_{2}\ \cdot H_{2}O]} }}=4,27\ \cdot 10^{-7}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b537959bb11038695c186d772b65ff7029b8922e)

![{\displaystyle K_{a2}=\ {\frac {\ \mathrm {[CO_{3}^{2-}]\ \cdot [H_{3}O^{+}]} }{\ \mathrm {[HCO_{3}^{-}]} }}=4,68\ \cdot 10^{-11}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/9f9bb2249f016de9f77dcf87227f72e9ac4eb424)













