Топ питань
Часова шкала
Чат
Перспективи
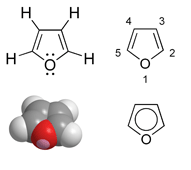
Фуран
хімічна сполука З Вікіпедії, вільної енциклопедії
Remove ads
Фура́н — гетероциклічна органічна сполука. Добувається, зазвичай, шляхом термічного розкладання пентозних матеріалів, наприклад целюлозних субстратів (деревина сосни). Фуран — це безбарвна легкозаймиста, досить нестабільна рідина з температурою кипіння близької до кімнатної. Є токсичною і може бути канцерогенною. Каталітичним гідруванням фурану на паладієвих каталізаторах добувають тетрагідрофуран.
Фуран вважається ароматичним тому, що одна з пар електронів на атомі кисню делокалізована в кільце, створюючи 4n+2 ароматичну систему (за правилом Гюккеля), аналогічно бензену. Через ароматичність молекула є плоскою з делокалізованими «ароматичними» зв‘язками. Друга пара електронів атому оксигену знаходиться в площині молекулярної системи. Суть sp2 гібридизації полягає в тому, щоб одна вільна пара оксигену належала π-орбіталі, і саме так, щоб вона могла взаємодіяти рамках π-системи.
Назва фурану походить від лат. furfur, що означає висівки.[1] Перша похідна фурану, яка була описана — 2-фуранова кислота, Карлом Вільгельмом Шеєле в 1780 році. Інша важлива похідна, фурфураль, представлена Йоганном Вольфгангом Деберайнером в 1831 і охарактеризована лише дев‘ять років по тому Джоном Стенхаусом. Сам фуран вперше був синтезований Генрихом Лімпріхтом в 1870 році, хоча той і назвав його "тетрафенолом”.[2][3]
Remove ads
Отримання
В промисловості фуран отримують декарбонілюванням фурфуролу, чи окисленням бутадієну в присутності мідного каталізатора:[4]
Також фуран отримують декарбоксилюванням 2-фуранкарбонової кислоти[5]:
Хімічні властивості
Узагальнити
Перспектива
Завдяки своїй ароматичності, поведінка фурану досить різноманітна, на відміну від більшості типових гетероциклічних етерів, наприклад тетрагідрофурану.
Електрофільне заміщення
Фуран більш реакційноздатний ніж бензен та тіофен в реакціях електрофільного заміщення, це пов'язано з електронно-донорним впливом гетероароматичного оксигену. Вивчення резонансних структур показує збільшення електронної густини в кільці, що призводить до зростання ймовірності електрофільного заміщення.
Разом з тим практично здійснити електрофільне заміщення в ядрі фурану дуже важко, оскільки він легко полімеризується (осмолюється) в присутності кислот. Так для нітрування фурану застосовують такі нетривіальні реагенти як тетранітрометан. Похідні, що містять акцепторні замісники (особливо у положенні 2) набагато стійкіші у кислому середовищі, зокрема фурфурол (2-форміл-фуран) може бути пробромований напряму.
Реакції приєднання
Фуран виступає дієном в реакції Дільса—Альдера з електронно-акцепторними дієнофілами, такими як етиловий ефір-(2E)-3-нітроакрилату.[6] Продуктом реакції є суміш ізомерів з переважанням ендо-ізомеру:
Також фуран може приєднувати і молекули які не є типовими дієнофілами, наприклад молекулу брому
У присутності нікелю приєднує водень з утворенням тетрагідрофурану[5].
Реакції окиснення
При окисненні фурану утворюється малеїновий ангідрид. Окиснення проводиться в нейтральному або слаболужному середовищі. В якості окисника використовується дихромат калію або оксид хрому(VI):
Remove ads
Спектральні властивості та будова молекули
В ЯМР спектрах фурану сигнали протонів спостерігаються в регіоні типовому для ароматичних сполук що може бути додатковим підтвердженням ароматичності молекули.

Примітки
Посилання
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads