
Оксид азоту(I)
хімічна сполука / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Монооксид діазоту?
Підсумуйте цю статтю для 10-річної дитини
ПОКАЗАТИ ВСІ ЗАПИТАННЯ
Окси́д азо́ту(I), нітроге́н(I) окси́д — неорганічна сполука складу N2O. За звичайних умов є безбарвним газом із солодкуватим запахом. Він може підтримувати горіння; проявляє слабкі окисні та відновні властивості.
Коротка інформація Ідентифікатори, Номер CAS ...
| Оксид азоту(I) | |
|---|---|
Резонансна структура оксиду | |
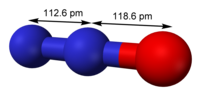 | |
| Інші назви | геміоксид азоту |
| Ідентифікатори | |
| Номер CAS | 10024-97-2 |
| Номер EINECS | 233-032-0 |
| DrugBank | 06690 |
| KEGG | D00102 і C00887 |
| Назва MeSH | D01.362.635.625, D01.625.550.550 і D01.650.550.587.650 |
| ChEBI | 17045 |
| RTECS | QX1350000 |
| Код ATC | N01AX13 |
| SMILES | N#[N+][O-][1] |
| InChI | InChI=1S/N2O/c1-2-3 |
| Номер Бельштейна | 8137358 |
| Номер Гмеліна | 2153410 |
| Властивості | |
| Молекулярна формула | N2O |
| Молярна маса | 44,012 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Запах | солодкуватий |
| Густина | 1,799 г/л[2] |
| Тпл | -90,8 °C[2] |
| Ткип | -88,49 °C[2] |
| Діелектрична проникність (ε) | 1,00104 (20 °C) |
| Показник заломлення (nD) | 1,238 |
| В'язкість | 10,0μПа·с (200 °K) 15,0μПа·с (300 °K) 19,4μПа·с (400 °K) 23,6μПа·с (500 °K) 27,4μПа·с (600 °K) |
| Структура | |
| Дипольний момент | 0,16083 D |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
81,6 кДж/моль |
| Ст. ентропія S 298 |
220,0 Дж/(моль·K) |
| Теплоємність, c p |
38,6 Дж/(моль·K) |
| Небезпеки | |
| ГДК (Україна) | 90 мг/м³ |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Закрити
Ця стаття про оксид азоту складу N2O. Про інші сполуки цього ряду див. Оксиди азоту.
Речовина застосовується у медицині для короткочасного наркозу, а також як піноутворювач у харчовій промисловості.