
Ozon
đơn chất / From Wikipedia, the free encyclopedia
Ozon (O3) là một phân tử chất vô cơ với công thức hóa học O
3. Nó là một chất khí màu xanh lam nhạt, có mùi hăng đặc biệt. Nó là một dạng thù hình của oxy kém bền hơn nhiều so với dạng nguyên tử O
2, bị phá vỡ trong bầu khí quyển thấp hơn thành O
2 (đioxy). Ozon được hình thành từ đioxy do tác động của tia cực tím (UV) và phóng điện trong bầu khí quyển Trái Đất. Nó hiện diện với nồng độ rất thấp trong suốt tầng sau, với nồng độ cao nhất ở tầng ozon của tầng bình lưu, nơi hấp thụ hầu hết bức xạ cực tím (UV) của Mặt Trời.
Bài viết này cần thêm chú thích nguồn gốc để kiểm chứng thông tin. |
| Ozone | |||
|---|---|---|---|
| |||
 | |||
| Danh pháp IUPAC | Ozone | ||
| Tên hệ thống | Trioxygen | ||
| Tên khác | 2λ4-trioxidiene; catena-trioxygen | ||
| Nhận dạng | |||
| Số CAS | 10028-15-6 | ||
| PubChem | 24823 | ||
| Số EINECS | 233–069–2 | ||
| MeSH | Ozone | ||
| ChEBI | 25812 | ||
| Số RTECS | RS8225000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| Tham chiếu Gmelin | 1101 | ||
| UNII | 66H7ZZK23N | ||
| Thuộc tính | |||
| Công thức phân tử | O3 | ||
| Bề ngoài | Colourless to pale blue gas[1] | ||
| Mùi | Pungent[1] | ||
| Khối lượng riêng | 2.144 mg cm−3 (at 0 °C) | ||
| Điểm nóng chảy | −192,2 °C; 81,0 K; −313,9 °F | ||
| Điểm sôi | −112 °C; 161 K; −170 °F | ||
| Độ hòa tan trong nước | 1.05 g L−1 (at 0 °C) | ||
| Độ hòa tan trong other solvents | Very soluble in CCl4, sulfuric acid | ||
| Áp suất hơi | 55.7 atm[2] (Lỗi Lua trong Mô_đun:Convert tại dòng 328: attempt to compare number with nil.)[lower-alpha 1] | ||
| MagSus | +6.7·10−6 cm³/mol | ||
| Chiết suất (nD) | 1.2226 (liquid), 1.00052 (gas, STP, 546 nm—note high dispersion)[3] | ||
| Cấu trúc | |||
| Nhóm không gian | C2v | ||
| Tọa độ | Digonal | ||
| Hình dạng phân tử | Dihedral | ||
| Lai hóa quỹ đạo | sp2 for O1 | ||
| Mômen lưỡng cực | 0.53 D | ||
| Nhiệt hóa học | |||
| Enthalpy hình thành ΔfH | 142.67 kJ mol−1 | ||
| Entropy mol tiêu chuẩn S | 238.92 J K−1 mol−1 | ||
| Các nguy hiểm | |||
| NFPA 704 |
| ||
| PEL | TWA 0.1 ppm (0.2 mg/m³)[1] | ||
| REL | C 0.1 ppm (0.2 mg/m³)[1] | ||
| IDLH | 5 ppm[1] | ||
| Ký hiệu GHS |      | ||
| Báo hiệu GHS | Danger | ||
| Chỉ dẫn nguy hiểm GHS | H270, H314 | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
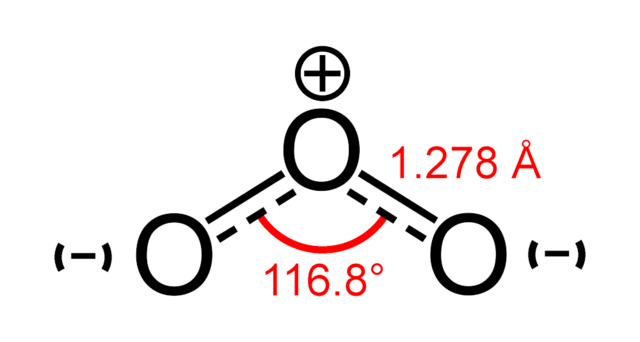
Mùi của ozon gợi nhớ đến clo và nhiều người có thể phát hiện được ozon ở nồng độ nhỏ nhất là 0,1 ppm trong không khí. Cấu trúc O3 của ozon được xác định vào năm 1865. Phân tử này sau đó đã được chứng minh là có cấu trúc uốn cong và thuận từ yếu. Ở điều kiện tiêu chuẩn, ozon là một chất khí màu xanh lam nhạt, ngưng tụ ở nhiệt độ lạnh thành chất lỏng màu xanh lam đậm và cuối cùng là chất rắn màu tím đen. Tính không ổn định của ozon đối với đioxy phổ biến hơn là cả khí đặc và ozon lỏng có thể bị phân hủy bùng nổ ở nhiệt độ cao hoặc nóng lên nhanh đến điểm sôi.[4] Do đó nó chỉ được sử dụng cho mục đích thương mại với nồng độ thấp.
Ozon là một chất oxy hóa mạnh (hơn nhiều so với oxy) và có nhiều ứng dụng trong công nghiệp và tiêu dùng liên quan đến quá trình oxy hóa. Tuy nhiên, cùng một tiềm năng oxy hóa cao này lại gây ra ozon phá hủy các mô niêm mạc và hô hấp ở động vật và cả các mô ở thực vật, trên nồng độ khoảng 0,1 ppm. Trong khi điều này làm cho ozon trở thành một chất gây ô nhiễm và nguy hiểm hô hấp mạnh gần mặt đất, nồng độ cao hơn trong tầng ozon (từ 2 đến 8 ppm) là có lợi, ngăn chặn tia cực tím có hại đến bề mặt Trái đất.
Một số thiết bị điện có thể sản sinh ra ozon mà con người có thể ngửi thấy dễ dàng. Điều này đặc biệt đúng với các thiết bị sử dụng điện cao áp, như ti vi và máy photocopy. Các động cơ điện sử dụng chổi quét cũng có thể sản sinh ozon do sự đánh lửa lặp lại bên trong khối. Các động cơ lớn, ví dụ những chiếc được sử dụng cho máy nâng hay máy bơm thủy lực, sản sinh nhiều ozon hơn các động cơ nhỏ.
Mật độ tập trung cao nhất của ozon trong khí quyển nằm ở tầng bình lưu(khoảng 20 đến 50 km tính từ mặt đất), trong khu vực được biết đến như là tầng ozon. Tại đây, nó lọc phần lớn các tia cực tím từ Mặt Trời, là tia có thể gây hại cho phần lớn các loại hình sinh vật trên Trái Đất. Phương pháp tiêu chuẩn để đo lượng ozon trong khí quyển là sử dụng đơn vị Dobson (DU). ozon sử dụng trong công nghiệp được đo bằng ppm (ví dụ các giới hạn phơi nắng của OSHA), và phần trăm theo khối lượng hay trọng lượng.


