热门问题
时间线
聊天
视角
硒酸
化合物 来自维基百科,自由的百科全书
Remove ads
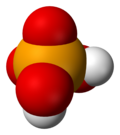
硒酸是一种无机酸,化学式为H2SeO4。它是硒的含氧酸,它的结构可以更准确地被描述为(HO)2SeO2。
Remove ads
制备
由于三氧化硒的不稳定性,不像三氧化硫溶于水生成硫酸,通过在水中溶解三氧化硒得到硒酸是不切实际的。[1]相反地,硒酸必须通过氧化低价态的硒化合物来制取。
SeO2 + H2O2 → H2SeO4
无水硒酸被公认为晶体,它可以由硒酸的溶液在140°C (413 K; 284 °F)温度下真空蒸发。[3]
硒酸也可以通过亚硒酸(H2SeO3)被卤素(如氯气或溴)或高锰酸钾氧化制取。[4]然而,用氯气或者溴作为氧化剂会产生盐酸或者氢溴酸作为副产物,它们需要从溶液中去除,因为它们可以将硒酸还原成亚硒酸。[5]
另一种制备硒酸的方法是将单质硒在水中的悬浊液用氯气氧化:[4]
Se + 4 H2O + 3 Cl2 → H2SeO4 + 6 HCl
化学性质
类似硫酸,硒酸是一种强酸,有吸湿性,在水中溶解度很强。其浓溶液是粘稠的。已知硒酸有一水合物和二水合物。[4]一水合物的熔点在26°C,而二水合物的熔点在−51.7°C。[1]
硒酸的氧化性比硫酸强,50%硒酸能将氯离子氧化成氯气,而自身被还原成亚硒酸或二氧化硒(但氯气能够将稀亚硒酸氧化为硒酸):[4]
- H2SeO4 + 2 H+ + 2 Cl− → H2SeO3 + H2O + Cl2
硒酸在200°C以上分解,放出氧气,自身被还原成亚硒酸:[4]
- 2 H2SeO4 → 2 H2SeO3 + O2
硒酸可以和钡盐反应生成沉淀BaSeO4,沉淀和硫酸钡的性质类似。总体上说,硒酸盐和硫酸盐的性质相似,但是在水中的溶解性更好。许多硒酸盐有相同的、和硫酸盐一致的晶体结构。[1]
- H2SeO4 + 2 HSO3F → SeO2F2 + 2 H2SO4
热的浓硒酸可以溶解单质金,产生红黄色的硒酸金(III):[6]
- 2 Au + 6 H2SeO4 → Au2(SeO4)3 + 3 H2SeO3 + 3 H2O
后来,人们发现这种红黄色的物质其实是Au2(SeO3)2(SeO4),其中硒的价态被IR和NMR确定。因此,其反应方程式应该为:[7]
- 2 Au + 4 H2SeO4(浓) → Au2(SeO3)2(SeO4) + H2SeO3 + 3 H2O
Remove ads
参考资料
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads