Loading AI tools
来自维基百科,自由的百科全书
溴化亞錫是一種無機化合物,由錫和溴組成,化學式 SnBr2。 在這個化合物里,錫的氧化態為 +2 。二價錫的化合物穩定是惰性電子對效應造成的。[1]
| 溴化亞錫 | |
|---|---|
| |
| 別名 | 二溴化錫 溴化錫(II) |
| 識別 | |
| CAS號 | 10031-24-0(無水) 127294-36-4(二水) |
| PubChem | 66224 |
| ChemSpider | 59609 |
| SMILES |
|
| InChI |
|
| InChIKey | ZSUXOVNWDZTCFN-NUQVWONBAM |
| EINECS | 233-087-0 |
| 性質 | |
| 化學式 | SnBr2 |
| 摩爾質量 | 278.518 g/mol g·mol⁻¹ |
| 外觀 | 黃色固體 |
| 密度 | 5.12 g/cm3,固態 |
| 熔點 | 215 °C(488 K) |
| 沸點 | 639 °C(912 K) |
| 結構 | |
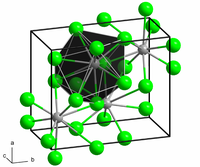
| 晶體結構 | 類似 PbCl2 |
| 危險性 | |
| 歐盟分類 | 未列出 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氣態 SnBr2 分子是一種角形的分子,與 SnCl2 在氣態的時候一樣。 Br-Sn-Br 的鍵角為 95° , Sn-Br 的鍵長則為 255pm。[2] 有證據表明它會二聚。[3] 固態溴化亞錫的結構類似SnCl2和PbCl2。錫與五個溴原子配位,形狀類似三角雙錐。[4]
溴化亞錫可以由金屬錫和HBr反應而成,蒸餾出H2O/HBr並冷卻:[5]
不過,如果接觸氧氣,這個反應會生成四溴化錫。
SnBr2 可溶於供體溶劑,例如丙酮、吡啶和二甲基亞碸,得到錐形加合物。 [5]
它有很多種水合物,如: 2SnBr2·H2O、3SnBr2·H2O 和 6SnBr2·5H2O 。它們的固相中的錫的配位是扭曲的三角柱,連接6個溴原子,且Br或H2 O覆蓋1或2個面。 [1]
當它溶於HBr時,三角錐型的 SnBr3− 離子會被產生。[1]
和 SnCl2 一樣,溴化亞錫也是一種還原劑。它和溴代烴反應,生成烷基三溴化錫。[6] 例如:
溴化亞錫是一種路易斯酸,可以和配體如:三甲胺形成加合物如: NMe3.SnBr2 和 2NMe3.SnBr2。 [7] 它也可以和同時路易斯酸和路易斯鹼形成加合物,例如 F3B.SnBr2.NMe3 ,路易斯酸是三氟化硼,而路易斯鹼則是三甲胺。 [8]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.