砷(英語:Arsenic),舊稱砒,是一種化學元素,化學符號為As,原子序數為33,原子量為7001749215950000000♠74.921595 u。砷分布在多種礦物中,通常與硫和其它金屬元素共存,也有純的元素晶體。艾爾伯圖斯·麥格努斯在1250年首次對砷進行了記載[3]。砷是一種非金屬元素。單質以灰砷、黑砷和黃砷這三種同素異形體的形式存在,但只有灰砷在工業上具有重要的用途。
Quick Facts 外觀, 概況 ...
砷 33As|
|
| 外觀 |
|---|
銀灰色
 |
| 概況 |
|---|
| 名稱·符號·序數 | 砷(Arsenic)·As·33 |
|---|
| 元素類別 | 類金屬 |
|---|
| 族·週期·區 | 15·4·s |
|---|
| 標準原子質量 | 74.921595(6)[1] |
|---|
| 電子排布 | [Ar] 3d104s24p3
2, 8, 18, 5
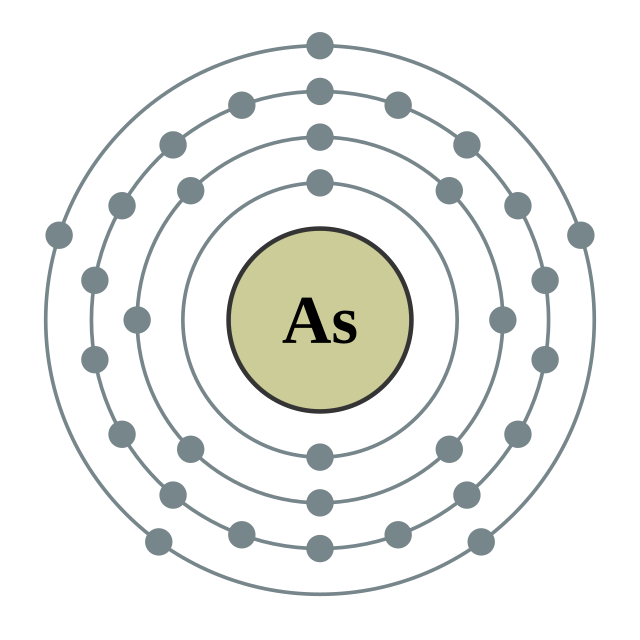 砷的電子層(2, 8, 18, 5) 砷的電子層(2, 8, 18, 5) |
|---|
| 歷史 |
|---|
| 分離 | 艾爾伯圖斯·麥格努斯(1250年) |
|---|
| 物理性質 |
|---|
| 物態 | 固態 |
|---|
| 密度 | (接近室溫)
5.727 g·cm−3 |
|---|
| 熔點時液體密度 | 5.22 g·cm−3 |
|---|
| 昇華點 | 887 K,615 °C,1137 °F |
|---|
| 三相點 | 1090 K(817 °C),3628 kPa |
|---|
| 臨界點 | 1673 K,? MPa |
|---|
| 熔化熱 | (灰砷) 24.44 kJ·mol−1 |
|---|
| 汽化熱 | ? 34.76 kJ·mol−1 |
|---|
| 比熱容 | 24.64 J·mol−1·K−1 |
|---|
蒸氣壓
| 壓/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| 溫/K
|
553
|
596
|
646
|
706
|
781
|
874
|
|
| 原子性質 |
|---|
| 氧化態 | 5, 3, 2, 1, -3
(酸性) |
|---|
| 電負性 | 2.18(鮑林標度) |
|---|
| 電離能 | 第一:947.0 kJ·mol−1
第二:1798 kJ·mol−1
第三:2735 kJ·mol−1
(更多) |
|---|
| 原子半徑 | 119 pm |
|---|
| 共價半徑 | 119±4 pm |
|---|
| 范德華半徑 | 185 pm |
|---|
 砷的原子譜線 砷的原子譜線 |
| 雜項 |
|---|
| 晶體結構 | 三方[2] |
|---|
| 磁序 | 抗磁性 |
|---|
| 電阻率 | (20 °C)333 n Ω·m |
|---|
| 熱導率 | 50.2 W·m−1·K−1 |
|---|
| 楊氏模量 | 8 GPa |
|---|
| 體積模量 | 22 GPa |
|---|
| 莫氏硬度 | 3.5 |
|---|
| 布氏硬度 | 1440 MPa |
|---|
| CAS號 | 7440-38-2 |
|---|
| 同位素 |
|---|
主條目:砷的同位素
|
Close
砷可用於合金的製造,比如生產銅的強化合金或是添加到製造車用鉛酸蓄電池的合金中。[4]製造半導體電子器件時用砷作為摻雜劑合成n形半導體材料,摻雜了硅的光電子化合物砷化鎵是在使用中最常見的半導體。砷和它的化合物,特別是三氧化二砷(砒霜)用於合成農藥(用於處理木材產品)、除草劑和殺蟲劑。但這些方面的應用正在逐漸消失[5]。
雖然有少數幾種細菌能夠將砷化合物作為呼吸代謝物[6],但是對於多細胞生物而言砷是有毒物質。受砷污染的地下水是影響全世界幾百萬人的環境問題。


