热门问题
时间线
聊天
视角
利伐沙班
来自维基百科,自由的百科全书
Remove ads
利伐沙班(英語:Rivaroxaban),以Xarelto等品牌銷售,是一種用於治療和預防血栓的抗凝藥物(血液稀釋劑)。具體而言,它用於治療深靜脈血栓形成和肺栓塞,並預防心房顫動和髖關節或膝關節手術後的血栓。它是口服的。[6]
常見的副作用包括出血。[6]其他嚴重的副作用可能包括脊髓硬膜外血腫和過敏性休克。[6]目前尚不清楚在懷孕和哺乳期間使用是否安全。[1]與華法林相比,它與其他藥物的相互作用較少。[7]它通過阻斷凝血蛋白凝血因子Xa的活性起作用。[6]
利伐沙班於2007年獲得專利,並於2011年在美國獲批用於醫療用途。[8]在美國,直到 2024 年它才能作為仿製藥使用。[9][10]它被列入世界衛生組織基本藥物標準清單里。[11]在2019年,它是美國第91種最常用的處方藥,有超過800萬張處方。[12][13]
Remove ads
歷史
利伐沙班最初由拜耳公司開發的。[14]在美國,它由楊森製藥(強生公司的一部分)銷售。[14]它是第一個口服的直接凝血因子Xa抑制劑。[15]
醫用

在非瓣膜性心房顫動患者中,它在預防缺血性中風和栓塞事件方面似乎與華法林一樣有效。[16][17]與華法林相比,利伐沙班與嚴重和致命出血事件的發生率較低相關,儘管利伐沙班與消化道出血率較高有關。[18]
禁忌
由於與控制出血相關的困難,利伐沙班應在手術前至少24小時停用,然後在確定充分止血後立即重新開始。[20]
劑量建議不建議將利伐沙班與已知為強聯合CYP3A4/P-糖蛋白抑制劑的藥物合用,因為這會導致利伐沙班的血漿濃度顯着升高。[2][21]
不利影響
最嚴重的不良反應是出血,包括嚴重的內出血。[22][23][24]與華法林相比,利伐沙班的嚴重和致命出血事件發生率較低,但消化道出血發生率較高。[25]
截止2015年,上市後評估顯示肝毒性,需要進一步研究來量化這種風險。[26][27]在2015年,在FDA不良事件報告系統(AERS)的定期監測藥物中,利伐沙班被報告的嚴重傷害病例數最多。[28]
2014年10月,Portola Pharmaceuticals完成了andexanet alfa作為凝血因子Xa抑制劑的解毒劑且副作用少的I期和II期臨床試驗,並啟動了三期試驗。[29][30] Andexanet alfa於2018年5月獲得美國食品和藥物管理局的批准,商品名為 Andexxa。[31][32]
作用機制
利伐沙班抑制凝血酶原酶複合物中游離和結合的凝血因子Xa。[33]它是一種選擇性直接凝血因子Xa抑制劑,起效時間為2.5至4小時。[34]凝血因子Xa的抑制會中斷凝血級聯的內在和外在途徑,從而抑制凝血酶的形成和血栓的發展。利伐沙班不抑制凝血酶(激活的凝血因子II),並且已證明對血小板沒有影響。[4]它允許可預測的抗凝和劑量調整以及常規凝血監測;[4]不需要飲食限制。[35]
普通肝素、低分子量肝素和磺達肝素也通過與循環抗凝血酶結合而間接抑制凝血因子Xa的活性並且必須通過注射,而口服活性華法林、苯丙香豆素和醋硝香豆素是維生素K拮抗劑,可降低許多凝血因子,包括凝血因子Xa。[36]
利伐沙班在廣泛的患者(年齡、性別、體重、種族)中具有可預測的藥物代謝動力學,並且在八倍劑量範圍(5-40mg)內具有平坦的劑量反應。[37]口服生物利用度是劑量依賴性的。[38]10mg以下的利伐沙班劑量可以在有或沒有食物的情況下服用,因為它顯示出高生物利用度,而與是否食用食物無關。[39]如果以15mg或20mg口服劑量給予利伐沙班,則需要與食物一起服用以幫助藥物吸收並達到適當的生物利用度(≥80%)。[39]
Remove ads
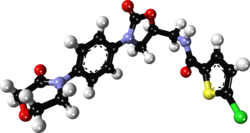
化學

利伐沙班與抗生素利奈唑胺有着驚人的結構相似性:兩種藥物具有相同的噁唑烷酮衍生核心結構。[40]因此,利伐沙班已被研究了任何可能的抗菌作用和線粒體毒性的可能性,線粒體毒性是長期使用利奈唑胺的已知併發症。[41]研究發現,利伐沙班及其代謝物都對革蘭氏陽性菌沒有任何抗生素作用。[來源請求]至於線粒體毒性,2008年之前發表的體外研究發現風險很低。[40]
社會與文化
根據美國最大的藥房福利管理公司快捷藥方的數據,使用利伐沙班而非華法林的成本要高出70倍。[4]截至2016年,拜耳公司聲稱該藥物已在130個國家獲得許可,超過2300萬患者接受了治療。[42]
在2008年9月,加拿大衛生部授予利伐沙班的上市許可,用於預防接受選擇性全髖關節置換術或全膝關節置換術患者的靜脈血栓。[43]
同月,歐盟委員會也授予利伐沙班的上市許可,用於預防接受擇期髖關節和膝關節置換術的成人靜脈血栓栓塞症。[44][3]
在2011年7月1日,美國食品和藥物管理局批准利伐沙班在接受髖關節和膝關節置換手術的成人中預防可能導致肺栓塞的深靜脈血栓形成。
在2019年3月25日,在美國有25,000多起關於利伐沙班的訴訟以7.75億美元和解,以支付給受影響的人。原告指責製藥商沒有警告出血風險,聲稱如果向醫生和患者提供足夠的信息,他們的傷害是可以避免的。[46]
研究
杜克大學醫學院的研究人員被指控隱瞞用於評估利伐沙班的臨床數據。[47]杜克大學在一項名為ROCKET AF試驗的臨床試驗中測試了利伐沙班。[48]該臨床試驗於2011年發表在《新英格蘭醫學雜誌》上[49]並由時任FDA專員羅伯特·卡利夫領導,[50][49]發現利伐沙班在降低房顫患者缺血性卒中的可能性方面比華法林更有效。[49]該研究的有效性在2014年受到質疑,當時製藥贊助商拜耳公司和強生公司透露所使用的INRatio血液監測設備運行不正常。[47][48]杜克團隊隨後在2016年2月發表的一項分析發現,這對於試驗的療效和安全性沒有顯着影響。[51]
臨床試驗中少數族裔的代表性不足已經被經注意到。與華法林相比,不同種族亞組的療效和安全性相似。[49]
參考文獻
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads