四氟一氧化氙(化學式:XeOF4)是稀有氣體氙生成的鹵氧化物之一,屬於其中比較穩定的一個,可以長期儲存於鎳制的容器中。四氟一氧化氙是六氟化氙水解不完全的產物,它可以進一步水解為二氟二氧化氙,最終生成三氧化氙。
| 四氟一氧化氙 | |
|---|---|

| |
| |
| 別名 | 四氟氧化氙、氟氧化氙 |
| 識別 | |
| CAS號 | 13774-85-1 |
| ChemSpider | 10326200 |
| SMILES |
|
| InChI |
|
| InChIKey | ONRYXFFHIXYZMZ-UHFFFAOYAY |
| 性質 | |
| 化學式 | XeOF4 |
| 摩爾質量 | 223.23 g·mol⁻¹ |
| 外觀 | 無色液體[1][2] |
| 密度 | 3.17 g/cm3 (液) |
| 熔點 | -46.2°C[3] |
| 溶解性(水) | 與水反應 |
| 結構 | |
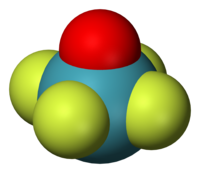
| 分子構型 | 四方錐[4][1] |
| 危險性 | |
| 歐盟危險性符號 未列明 | |
| 相關物質 | |
| 相關化學品 | 六氟化氙、三氧化氙 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
四氟一氧化氙分子為四方錐構型,Xe-F鍵長1.902 ± 0.002 Å,Xe-O鍵長1.708 ± 0.007 Å。[5]它有部分電離,加入氟化銫或氟化銣會使電導率劇烈增大。[6]
製備
- XeF6 + H2O → XeOF4 + 2HF
把六氟化氙封裝在石英容器中,讓六氟化氙與二氧化矽緩慢反應,也能生成四氟一氧化氙。[2]
- 2XeF6 + SiO2 → 2XeOF4 + SiF4
- NaNO3 + XeF6 → NaF + XeOF4 + NO2F
通過XeF6和POF3在−196 °C(−320.8 °F;77.1 K)下的反應,可以高產率的獲得四氟一氧化氙。[9]
將氙、氟和氧的混合物加熱到235°C可以得到四氟化氙和四氟一氧化氙。這個混合物在0°C下真空蒸餾可以得到純淨的四氟一氧化氙液體。[10]
反應
XeOF4可以繼續水解:[11]
液態的XeOF4有兩性,可以和強路易斯鹼(如氟化銫)和強路易斯酸(如五氟化銻)形成配合物。[12]它和五氟化銻反應的產物有XeOF3SbF6和XeOF3Sb2F11,都是含有XeOF3+離子的白色固體。[13]它和亞硝酰氟反應,生成NOXeOF5,其中含有五角錐形的XeOF5-離子。[14]它可以和二氟化氙形成1:1的加合物,這種加合物和XeF2·IF5同構。[15]
XeOF4和XeO3的反應可用來製備XeO2F2。[16]
四氟一氧化氙可被過量的氫在300°C時還原為氙。這是一個定量反應,可以用這個方法分析XeOF4:[17]
- XeOF4 + 3H2 → Xe + H2O + 4HF
參見
- 氙的其他鹵氧化物:
參考資料
擴展閱讀
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
