
硫化物
維基百科,自由的 encyclopedia
無機化學中,硫化物指電正性較強的金屬或非金屬與硫形成的一類化合物。大多數金屬硫化物都可看作氫硫酸的鹽。由於氫硫酸是二元弱酸,因此硫化物可分為酸式鹽(HS−,氫硫化物)、正鹽(S2−)和多硫化物(Sn2−)三類。
Quick Facts 硫化物, 識別 ...
| 硫化物 | |
|---|---|
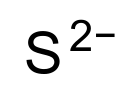 | |
| 系統名 Sulfide(2−)[1] (additive), recommended name Sulfanediide (substitutive),[1] not common, rarely used, sometimes generated by automated nomenclature software in organic chemistry | |
| 識別 | |
| CAS號 | 18496-25-8 |
| PubChem | 29109 |
| ChemSpider | 27079 |
| SMILES |
|
| ChEBI | 15138 |
| 性質 | |
| 化學式 | S |
| 摩爾質量 | 32.07 g·mol−1 |
| 相關物質 | |
| 其他陰離子 | 氧化物 硒化物 碲化物 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
Close
有機化學中,硫化物(英文:Sulfide)指含有二價硫的有機化合物。根據具體情況的不同,有機硫化物可包括:硫醚(R-S-R)、硫酚/硫醇(Ar/R-SH)、硫醛(R-CSH)、硫代羧酸(S取代羧基中的一個或兩個O,如R-CO-SH、R-CS-OH、R-CS-SH)和二硫化物(R-S-S-R)等。參見有機硫化合物。