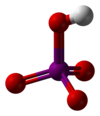
高碘酸是碘的最高含氧酸,其中碘以+7氧化態存在。它可以以兩種形式存在:化學式為H5IO6的正高碘酸和化學式為HIO4的偏高碘酸。
| 高碘酸 | |||
|---|---|---|---|
| |||
| |||

| |||
| 別名 | 碘(VII)酸 | ||
| 識別 | |||
| CAS編號 | 10450-60-9(正高碘酸) 13444-71-8(偏高碘酸) | ||
| ChemSpider | 23622 (正高碘酸), 58684 (偏高碘酸) | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | TWLXDPFBEPBAQB-UHFFFAOYSA-N | ||
| UN編號 | UN3085 | ||
| 性質 | |||
| 化學式 | HIO 4(偏高碘酸) H 5IO 6(正高碘酸) | ||
| 摩爾質量 | 190.91 g/mol (HIO 4) 227.941 g/mol (H 5IO 6) g·mol⁻¹ | ||
| 外觀 | 無色晶體 | ||
| 熔點 | 128.5 °C(402 K)([1]) | ||
| 溶解性 | 溶於水、醇 | ||
| 危險性 | |||
GHS危險性符號   
| |||
| GHS提示詞 | Danger | ||
| H-術語 | H271, H314, H372, H400 | ||
| P-術語 | P210, P260, P273, P303+361+353, P305+351+338 | ||
| NFPA 704 | |||
| 相關物質 | |||
| 其他陰離子 | |||
| 其他陽離子 | |||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
高碘酸由海因里希·古斯塔夫·馬格努斯和CF Ammermüller於1833年發現。[2]
合成
現代工業規模生產涉及碘酸鈉溶液在鹼性條件下的氧化,或者在PbO
2陽極上進行電化學氧化,或者通過氯處理:[3]
- IO−
3 + 6 HO−
- 2 e−
→ IO5−
6 + 3 H
2O (為方便省略抗衡離子) E° = -1.6 V[4] - IO−
3 + 6 HO−
+ Cl
2 → IO5−
6 + 2 Cl−
+ 3 H
2O
原高碘酸在減壓下加熱至100℃可脫水得到偏高碘酸。
- H
5IO
6 ⇌ HIO
4 + 2 H
2O
進一步加熱至約150 °C得到五氧化二碘(I
2O
5),而不是預期的酸酐[七氧化二碘(I
2O
7)]。偏高碘酸也可由各種正高碘酸鹽經稀硝酸處理製得。[5]
性質
正高碘酸有多個酸解離常數。[6][7] 偏高碘酸的pKa尚未確定。
- H
5IO
6 ⇌ H
4IO−
6 + H+
, pKa = 3.29
- H
4IO−
6 ⇌ H
3IO2−
6 + H+
, pKa = 8.31
- H
3IO2−
6 ⇌ H
2IO3−
6 + H+
, pKa = 11.60
存在兩種形式的高碘酸,因此形成兩種類型的高碘酸鹽。例如,偏高碘酸鈉NaIO4可以由HIO4合成,而正高碘酸鈉Na5IO6可以由H5IO6合成。
正高碘酸形成單斜晶體(空間群P21/n),由一個輕微變形的IO
6八面體通過橋接氫相互連接組成。五個I-O鍵距離在1.87-1.91 Å範圍內,一個I-O鍵距離為 1.78 Å。[8][9]
偏高碘酸的結構還包括IO
6八面體,但是它們通過順共棱與橋氧連接形成一維無限鏈。[10]
反應
像所有高碘酸鹽一樣,高碘酸可用於裂解各種1,2-雙官能基化合物。高碘酸會將鄰二醇裂解成兩個醛或酮片段(馬拉普拉德反應)。

這可用於確定碳水化合物的結構,因為高碘酸可用於打開糖環。該過程通常用於用熒光分子或其他標籤(如生物素)標記糖類。由於該過程需要連位二醇,因此高碘酸鹽氧化通常用於選擇性標記RNA的 3'-末端(核糖具有連位二醇)而不是DNA,因為去氧核糖沒有連位二醇。
高碘酸也被用作中等強度的氧化劑,例如在仲烯丙醇的Babler氧化反應中,通過化學計量的正高碘酸與催化劑PCC將其氧化成烯酮。[11]
參見
具有相似結構的化合物:
化學性質相似的化合物:
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.