
脑瘤
病症 / 维基百科,自由的 encyclopedia
脑瘤(英语:brain tumor)或称脑肿瘤,又名颅内肿瘤(intracranial tumor),是颅内的异常组织团块,其异常细胞不受控地生长和增殖[7][2]。脑瘤发生的组织包括了脑本身各种细胞(神经元、胶质细胞、淋巴组织以及血管)、脑神经(许旺细胞)、脑膜、头骨、脑下垂体以及由其它器官转移的转移性脑瘤[8][9]。
| 脑癌 | |
|---|---|
| 同义词 | Intracranial neoplasm |
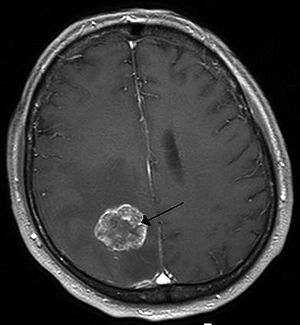 | |
| 肺癌转移到大脑右半球的核磁共振造影 | |
| 症状 | 随病变的脑区不同而出现不同的症状:头痛、癫痫发作、视觉出问题、呕吐、认知改变[1][2] |
| 类型 | 恶性、良性[2] |
| 肇因 | 通常未知[2] |
| 风险因子 | 神经纤维瘤病、接触氯乙烯、EBV、游离辐射[2][1][3] |
| 诊断方法 | CT,NMRI,活体组织切片[2][1] |
| 治疗 | 外科学、放射线疗法、化学疗法[1] |
| 药物 | 抗惊厥药(英语:Anticonvulsant)、地塞米松、呋塞米[1] |
| 预后 | 平均五年存活率 35% (美国)[4] |
| 盛行率 | 1.2百万神经系统癌症(2015年)[5] |
| 死亡数 | 229,000人(2015年)[6] |
| 分类和外部资源 | |
| 医学专科 | 神经外科、肿瘤学 |
| ICD-11 | 2A00 |
| DiseasesDB | 30781 |
| MedlinePlus | 007222、000768 |
| eMedicine | 779664 |
| [编辑此条目的维基数据] | |
脑瘤主要有两种类型:恶性肿瘤(癌症)、良性肿瘤(非癌症肿瘤)[2]。癌症肿瘤可再分为原发性脑瘤(英语:Primary_tumor)与继发性脑瘤(转移性脑瘤(英语:Brain_metastasis)),后者是由位于脑外的肿瘤扩散而来,又称为脑转移瘤[1]。
所有型态的脑瘤都会产生症状,因为脑瘤渐渐增大必会压住该处之神经,影响其功能,所以临床表现因部位不同[2],包含头痛、抽搐、视力问题、呕吐、意识改变[1]。典型的头痛为早晨时恶化,并伴随呕吐而头痛减缓[2]。其他特殊的症状包含行走、说话困难,以及感觉异常[1][3]。当疾病进展时,可能会失去意识(英语:Unconsciousness)[3]。在恶性脑瘤晚期,肿瘤细胞也会转移至身体其他脏器。
大部分脑瘤的发生原因不明[2],危险因子可能包括一些基因症候群如神经纤维瘤病(神经纤维瘤症后群),以及暴露于化学物质(如氯乙烯)、人类疱疹病毒第四型(Epstein-Barr virus)或游离辐射[2][1][3]。而对于手机使用产生的相关疑虑,目前缺乏明确证据[3]。在成人病患中最常见的原发性脑瘤是脑膜瘤(英语:meningiomas)和星状细胞瘤(英语:astrocytomas),后者如神经胶母细胞瘤(glioblastoma)[1];而在儿童病患中最常见的则是髓母细胞瘤(medulloblastoma)[3]。脑瘤的诊断以身体诊察搭配电脑断层扫描(computed tomography)或磁共振影像(magnetic resonance imaging)为主[2],之后会进行切片检查确认,再根据病理结果区分为不同等级或严重度(英语:Grading of the tumors of the central nervous system)[1]。
治疗方式可能综合包括手术、放射线疗法和化学疗法数种方式。若有抽搐情形可使用抗癫痫药物(英语:Anticonvulsant)。Dexamethasone 与Furosemide[注 1]。部分肿瘤成长较缓慢,仅需要长期追踪[1]。以病患的免疫系统作为治疗方式,目前仍然在研究中[2]。预后则依肿瘤型态而定[3]。神经胶细胞瘤通常预后较差,而脑膜瘤较好[3]。在美国,脑瘤平均五年存活率为33%[10][4]。
转移性脑瘤比原发性脑瘤常见,约有一半的转移性脑瘤来自肺癌[2]。全球每年发生原发性脑瘤的人数约为250,000人,占所有癌症少于2%[3]。在15岁以下儿童族群中,脑瘤在癌症发生率排名中仅次于急性淋巴性白血病[11]。在澳洲平均一个脑瘤个案所必须花费的金额为190万,为所有癌症之最[12]。