
蛋白质折叠
维基百科,自由的 encyclopedia
蛋白质折叠(英语:Protein folding)是蛋白质获得其功能性结构和构象的物理过程。通过这一物理过程,蛋白质从无规则卷曲折叠成特定的功能性三维结构[1]。在从mRNA序列翻译成线性的氨基酸链时,蛋白质都是以去折叠多肽或无规则卷曲的形式存在。
| 此条目需要扩充。 (2007年9月26日) |

| 未解决的化学问题:是否有可能仅透过序列和环境信息预测多肽序列的二级、三级和四级结构?还有逆蛋白质折叠问题:是否有可能设计一种多肽,在特定环境条件下使它采用给定的结构? |
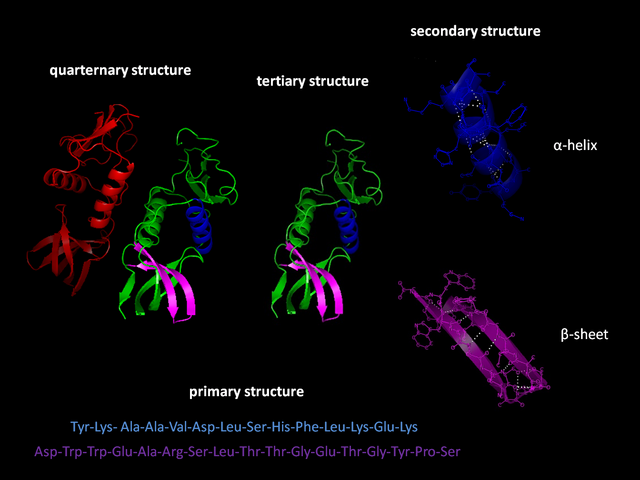
蛋白质的基本单位为氨基酸,而蛋白质的一级结构指的就是其氨基酸序列。蛋白质会由所含氨基酸残基的亲水性、疏水性、带正电、带负电等特性通过残基间的相互作用而折叠成一立体的三级结构。
根据克里斯琴·B·安芬森(1972年的诺贝尔化学奖得主)的研究,蛋白质可由加热或置于某些化学环境而变性,三级结构解体;而当环境回复到原本的状态时,蛋白质可于不到一秒的时间折叠至原先的立体结构,不论试验几次,蛋白质都仅此一种立体结构,于是安芬森提出一个结论:蛋白质分子的一级结构决定其立体结构(安芬森法则(英语:Anfinsen's dogma))[2]。
安芬森的研究结果非常重要,因为蛋白质的功能取决于其立体结构,而目前根据已知某基因序列可翻译获得对应蛋白质的氨基酸序列,即蛋白质的一级结构;如果从蛋白质的一级结构就能知道立体结构,那么即可直接从基因推测其编码蛋白质所对应的生物学功能。虽然蛋白质可在短时间中从一级结构折叠至立体结构,研究者却无法在短时间中从氨基酸序列计算出蛋白质结构,甚至无法得到准确的三维结构。因此,研究蛋白质折叠的过程,可以说是破译折叠密码的过程。
目前蛋白质的再折叠依然遵从先使用胍或脲变性,然后逐渐降低胍或者脲的浓度,也就是逐渐降低对蛋白质天然“回缩”能力的干扰。使其自然回到天然的最低能量状态。只是这个过程无法很好的控制肽链与肽链之间和肽链内部形成错误折叠的干扰。