
蛋白質摺疊
維基百科,自由的 encyclopedia
蛋白質摺疊(英語:Protein folding)是蛋白質獲得其功能性結構和構象的物理過程。通過這一物理過程,蛋白質從無規則捲曲摺疊成特定的功能性三維結構[1]。在從mRNA序列轉譯成線性的胺基酸鏈時,蛋白質都是以去摺疊多肽或無規則捲曲的形式存在。
| 此條目需要擴充。 (2007年9月26日) |

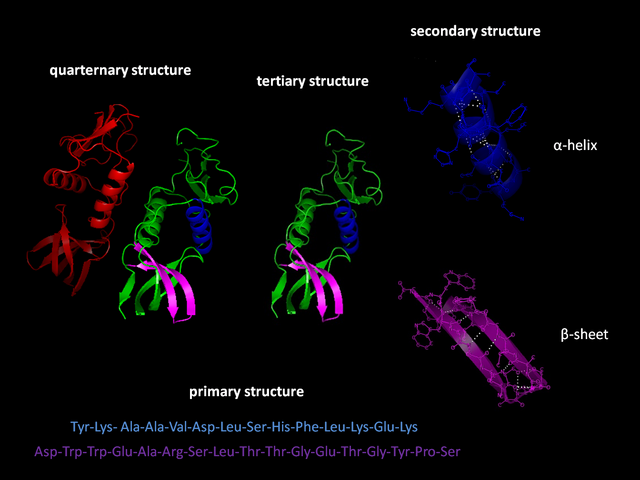
蛋白質的基本單位為胺基酸,而蛋白質的一級結構指的就是其胺基酸序列。蛋白質會由所含胺基酸殘基的親水性、疏水性、帶正電、帶負電等特性通過殘基間的相互作用而摺疊成一立體的三級結構。
根據克里斯琴·B·安芬森(1972年的諾貝爾化學獎得主)的研究,蛋白質可由加熱或置於某些化學環境而變性,三級結構解體;而當環境回復到原本的狀態時,蛋白質可於不到一秒的時間折疊至原先的立體結構,不論試驗幾次,蛋白質都僅此一種立體結構,於是安芬森提出一個結論:蛋白質分子的一級結構決定其立體結構(安芬森法則(英語:Anfinsen's dogma))[2]。
安芬森的研究結果非常重要,因為蛋白質的功能取決於其立體結構,而目前根據已知某基因序列可轉譯獲得對應蛋白質的胺基酸序列,即蛋白質的一級結構;如果從蛋白質的一級結構就能知道立體結構,那麼即可直接從基因推測其編碼蛋白質所對應的生物學功能。雖然蛋白質可在短時間中從一級結構摺疊至立體結構,研究者卻無法在短時間中從胺基酸序列計算出蛋白質結構,甚至無法得到準確的三維結構。因此,研究蛋白質摺疊的過程,可以說是破譯摺疊密碼的過程。
目前蛋白質的再摺疊依然遵從先使用胍或脲變性,然後逐漸降低胍或者脲的濃度,也就是逐漸降低對蛋白質天然「回縮」能力的干擾。使其自然回到天然的最低能量狀態。只是這個過程無法很好的控制肽鏈與肽鏈之間和肽鏈內部形成錯誤摺疊的干擾。