
關於一種手工藝,請見「
鋦瓷」。
鋦(英語:Curium),是一種人工合成的化學元素,其化學符號為Cm,原子序數為96,屬於錒系元素及超鈾元素,具有放射性,最長壽的同位素為鋦-247,半衰期達1560萬年。鋦在超鈾元素中排序第四,但其發現時間卻早於第三個超鈾元素鋂,於1944年7月由伯克利加州大學的格倫·西奧多·西博格等人首次專門合成出。其發現起初被列為機密,到1945年11月才公佈於世,並以研究放射性的科學家瑪麗·居禮和其丈夫皮埃爾·居禮命名。大部分的鋦是在核反應爐中通過對鈾或鈽進行中子撞擊產生的。每噸用過核燃料中含有大約20克鋦。
Quick Facts 外觀, 概況 ...
鋦 96Cm|
|
| 外觀 |
|---|
銀白色
 |
| 概況 |
|---|
| 名稱·符號·序數 | 鋦(Curium)·Cm·96 |
|---|
| 元素類別 | 錒系元素 |
|---|
| 族·週期·區 | 不適用·7·f |
|---|
| 標準原子質量 | [247] |
|---|
| 電子組態 | [Rn] 5f7 6d1 7s2
2, 8, 18, 32, 25, 9, 2
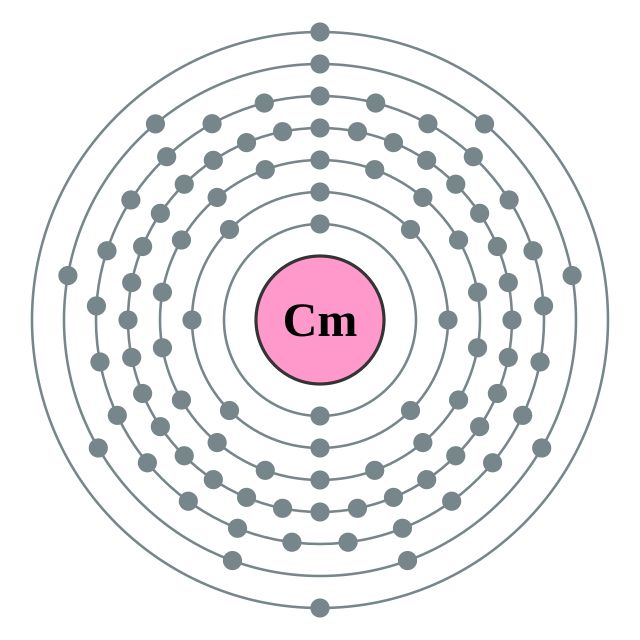 鋦的電子層(2, 8, 18, 32, 25, 9, 2) 鋦的電子層(2, 8, 18, 32, 25, 9, 2) |
|---|
| 歷史 |
|---|
| 發現 | 格倫·西奧多·西博格、Ralph A. James、阿伯特·吉奧索(1944年) |
|---|
| 物理性質 |
|---|
| 物態 | 固體 |
|---|
| 密度 | (接近室溫)
13.51 g·cm−3 |
|---|
| 熔點 | 1613 K,1340 °C,2444 °F |
|---|
| 沸點 | 3383 K,3110 °C,5630 °F |
|---|
| 熔化熱 | ? 15 kJ·mol−1 |
|---|
蒸氣壓
| 壓/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| 溫/K
|
1788
|
1982
|
|
|
|
|
|
| 原子性質 |
|---|
| 氧化態 | +3、+4、+5[1]、+6[2][5]
(兩性氧化物) |
|---|
| 電負度 | 1.3(鮑林標度) |
|---|
| 游離能 | 第一:581 kJ·mol−1 |
|---|
| 原子半徑 | 174 pm |
|---|
| 共價半徑 | 169±3 pm |
|---|
 鋦的原子譜線 鋦的原子譜線 |
| 雜項 |
|---|
| 晶體結構 | 六方密堆積 |
|---|
| 磁序 | 51 K時從反鐵磁性變為順磁性[6] |
|---|
| 電阻率 | 1.25[6] µ Ω·m |
|---|
| CAS編號 | 7440-51-9 |
|---|
| 同位素 |
|---|
主條目:鋦的同位素
| 同位素
|
豐度
|
半衰期(t1/2)
|
衰變
|
| 方式
|
能量(MeV)
|
產物
|
| 242Cm
|
人造
|
162.8 天
|
α
|
6.216
|
238Pu
|
| SF
|
–
|
–
|
| 243Cm
|
人造
|
29.1 年
|
α
|
6.169
|
239Pu
|
| ε
|
0.007
|
243Am
|
| SF
|
–
|
–
|
| 244Cm
|
人造
|
18.11 年
|
α
|
5.902
|
240Pu
|
| SF
|
–
|
–
|
| 245Cm
|
人造
|
8250 年
|
α
|
5.624
|
241Pu
|
| SF
|
–
|
–
|
| 246Cm
|
人造
|
4706 年
|
α
|
5.475
|
242Pu
|
| SF
|
–
|
–
|
| 247Cm
|
人造
|
1.56×107 年
|
α
|
5.354
|
243Pu
|
| 248Cm
|
人造
|
3.48×105 年
|
α
|
5.162
|
244Pu
|
| SF
|
–
|
–
|
| 250Cm
|
人造
|
8300 年?
|
SF
|
–
|
–
|
| α
|
5.170
|
246Pu
|
| β−
|
0.038
|
250Bk
| |
Close
鋦是一種銀白色的堅硬高密度金屬,熔點和沸點是錒系元素中較高的。鋦在標準溫度和壓力下具順磁性,並在冷卻後變為反鐵磁性;許多鋦化合物也具有磁性的轉變。鋦在化合物中的氧化態通常為+3和+4,而在溶液中主要呈+3態。鋦很容易被氧化,而形成的氧化物是鋦最常見的形態。鋦可以和各種有機化合物形成螢光錯合物,但不出現在任何細菌或古菌中。當攝入人體之後,鋦會累積在骨骼、肺部和肝臟中,並可致癌。
鋦的所有已知同位素都具有放射性,並具有較小的臨界質量(維持核連鎖反應所需的最低質量)。這些同位素主要放射α粒子,輻射釋放的熱量可以在放射性同位素熱電機中用來產生電力。然而由於量的稀少,以及製造費用的昂貴,鋦難以用來發電。鋦被用於製造更重的錒系元素,及在心律調節器中作為能源的238Pu。它也作為α粒子射源,被用在α粒子X射線光譜儀中。許多火星探測任務都使用該光譜儀來分析火星表面岩石的結構和成份,羅塞塔號的菲萊登陸器(Philae Lander)也用它來探測楚留莫夫-格拉希門克彗星的表面。


