热门问题
时间线
聊天
视角
放射性元素
没有稳定同位素的元素,即该类元素的所有同位素都具有放射性 来自维基百科,自由的百科全书
Remove ads
放射性元素(英語:radioactive element)是指原子核不穩定、具有放射性的化學元素。放射性元素的原子核會放射出游離輻射(電子、α粒子等次原子粒子和X射線、γ射線等高能光子),衰變成其他元素。[1]
每一種元素都有著多種同位素,其中大多具有放射性,會衰變成其他同位素,稱為放射性同位素;反之,原子核足夠穩定,不會發生放射性衰變的同位素,則稱為穩定同位素。而放射性元素是指沒有穩定同位素的元素,其所有同位素都具有放射性。元素週期表中,43號鎝和61號鉕以及所有原子序數為83(鉍)以上的元素都屬於放射性元素,而其餘原子序小於83的元素都具有至少1種穩定的同位素。[2]
每種放射性核種的核穩定性各不相同,發生衰變的半衰期也有長有短。通常質子或中子數為偶數的核種具有較高的穩定性[3],因此原子序(即質子數)為偶數的放射性元素,其最長壽同位素的半衰期大多比相鄰的奇數者來得長。例如90號元素釷和92號元素鈾的最長壽同位素釷232和鈾238分別具有140.5億年和44.68億年的長半衰期;而與之相鄰的89號錒和91號鏷,其最長壽同位素的半衰期則分別只有21.8年和32500年。原子序小於83的元素中唯二沒有穩定同位素的鎝和鉕,其原子序也都是奇數。
Remove ads
放射性元素列表
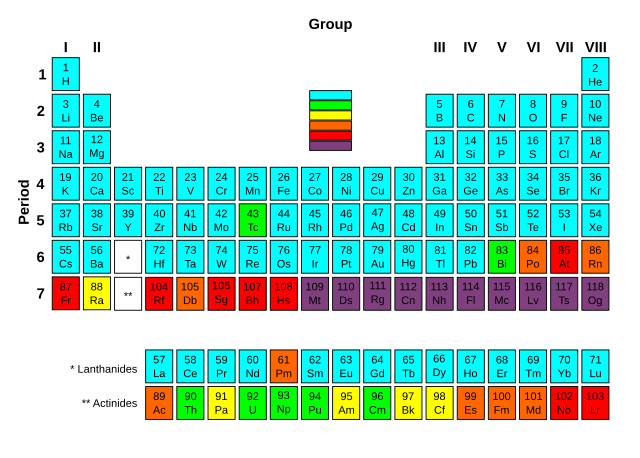
具有至少一種穩定同位素的元素
最穩定同位素之半衰期超過100萬年的放射性元素
最穩定同位素之半衰期介於800~34000年之間的放射性元素
最穩定同位素之半衰期介於1天~130年之間的強放射性元素
最穩定同位素之半衰期介於幾分鐘到1天內的強放射性元素
最穩定同位素之半衰期不到幾分鐘的強放射性元素。由於它們放射性極強且極度不穩定,目前對這些元素的性質所知甚少
以下表格列出所有已發現的放射性元素,表格中還有以下的項目:
- 原子序、名稱及元素符號都是用來區分各化學元素的基本訊息。
- 週期、族及分區表示該元素在週期表中的位置。
- 類別將元素依性質和在週期表中的位置做一簡單的分類。
- 標準原子量中根據該元素在自然界中各同位素的豐度比例,列出其平均原子量。自然界中豐度極低或不存在的元素則以其最長壽同位素之質量數表示。
- 最長壽同位素中列出該元素最長壽的同位素之質量數。
- 半衰期中列出該元素最長壽的同位素之半衰期。
- 存在情形依元素的來源分為三種:自然界中大量存在的原始元素、放射性原始元素的衰變產物(自然界中僅痕量存在)、自然界中不存在的人工合成元素。
- 豐度中列出該元素在地殼中的豐度(單位為mg/kg),地殼中不存在的元素則以-表示。
Remove ads
發現史
放射性元素的發現實際上早於放射性的發現。1789年德國化學家馬丁·克拉普羅特在瀝青鈾礦中發現了鈾[5],1828年瑞典化學家永斯·貝采利烏斯在釷石中發現了釷。[6]但當時「放射性」這一性質並不為人們所知,因此鈾和釷在發現後的很長一段時間內都只被看作是一般的重金屬元素。
1895年德國物理學家威廉·倫琴發現X射線後,激起許多學者開始研究這類新的、具有巨大穿透能力的放射線現象,放射性才被發現。
1896年法國物理學家亨利·貝克勒在研究磷光材料時發現鈾鹽會發射穿透性質的放射線,能夠使被黑色紙張包覆的底片感光,且該感光現象和磷光無關.因為使用非磷光材料的鈾鹽甚至鈾金屬,也會有一樣的效果。[7][8]1898年,德國化學家格哈德·施密特發現釷元素也具有這種放射線性質。[9][10][11]
1898年法國科學家居禮夫婦從瀝青鈾礦樣本中發現釙和鐳後,創造了「放射性」(radioactivity)[12]一詞來定義這種重元素發射高能游離輻射的性質[13](後來該詞的定義被擴展到所有元素)。在之後的幾年間科學家們陸續發現了多種放射性元素。
1899年法國科學家德比埃爾內從鈾礦渣中分離出放射性元素錒。[14][15]
1900年,德國物理學家弗里德里希·道恩發現,含鐳化合物會散發一種放射性氣體。[16][17][18][19]由於該氣體的光譜與氬、氪和氙相似,且該氣體呈化學惰性,因此威廉·拉姆齊於1904年猜測,該氣體可能是屬於惰性氣體一族的新元素。[20]該元素後來被命名為氡。
1917年,兩組科學家奧托·哈恩和莉澤·邁特納,以及德國和英國的弗雷德里克·索迪和約翰·克蘭斯登分別從瀝青鈾礦中分離出鏷。[21][22][23]
1937年,義大利物理學家卡羅·佩里爾和埃米利奧·塞戈雷從曾被用作迴旋加速器偏向板的鉬箔中分離出了第43號元素鎝。[24]它是第一個用人工合成的方法製得的放射性元素,因此命名為technetium(來自希臘文τεχνητός,意為「人造」)。[25]但1962年科學家發現自然界中也有痕量鎝的存在。[26]
1939年法國物理學家瑪格麗特·佩里在純化錒-227時在其衰變產物中發現了鍅。[27]鍅是最後一種從自然界中發現而不是在實驗室中人工合成出的元素。儘管有些元素最初是藉由人工合成的方式發現,但之後才發現它們也存在於自然界中,例如鈽、砈、錼、鎝和鉕。
1940年,戴爾·科爾森、肯尼斯·羅斯·麥肯西和埃米利奧·塞戈雷在迴旋加速器中以α粒子轟擊鉍原子合成出砈。[28]同年,埃德溫·麥克米倫和菲力普·艾貝爾森以中子照射鈾原子合成出了93號元素錼,這是第一種被發現的超鈾元素(原子序大於92號鈾的元素)。[29]隔年格倫·西奧多·西博格、約瑟夫·甘迺迪和埃德溫·麥克米倫合成出第二個超鈾元素鈽(原子序94)。[30]
1944年,格倫·西奧多·西博格和阿伯特·吉奧索等人合成並分離出96號元素鋦和95號元素鋂,它們是首批完全由人工合成的方式製得的純人造元素,不存在於自然界中。[31][32]
1945年,雅各布·馬林斯基、勞倫斯·格蘭丹寧和查爾斯·科耶爾在分析石墨反應爐中鈾燃料的分裂產物時發現了鉕,填補了週期表中61號元素的空白,至此所有原子序小於鈾的元素都已被發現。[33][34]
自1940年第一個超鈾元素錼被成功合成後,在之後的數十年間世界各國的科學家們陸續合成出多種原子序更大的超鈾元素。其中104到109號超重元素的命名曾引起很大的爭論,這些爭論從1960年代開始一直到1997年才解決(參見超鐨元素爭議)。[35][36]隨著新發現元素的原子序逐步增大,原子核的穩定性也愈低,更重元素的合成及觀測難度也因此愈高。科學家們至今仍藉由人工核反應力圖發現更多的新元素。
目前最新發現的元素為2010年合成出的鿬(Tennessine, Ts)[37],而目前發現原子序最大的元素則是118號的鿫(Oganesson, Og),於2002年合成出。[38][39]
另外,83號元素鉍長久以來一直被認為是最重的穩定元素,但2003年科學家發現其具有極其微弱的放射性,半衰期超過宇宙年齡的十億倍。[40]故82號的鉛取而代之成為了原子序最大的穩定元素。
Remove ads
存在
所有原子序數小於95(鋂)的放射性元素在自然界中都可找到其存在,稱為天然放射性元素。自然界中最普遍、豐度最高的放射性元素有三個:分別為釷、鈾和鉍等三種原始放射性元素,這三個元素都有一個或多個半衰期極長的放射性同位素,發生衰變的速率非常緩慢。因此雖然這些放射性元素的原子在太陽系形成之前、恆星核合成時即產生,在經歷數十億年後仍得以相當的量存留到現在。其中釷和鈾的衰變過程構成了現今自然界中最主要的三條衰變鏈,分別是以釷-232為母體的釷衰變鏈、以鈾-238為母體的鈾衰變鏈和以鈾-235為母體的錒衰變鏈,這三條衰變鏈的最終產物分別是穩定的鉛-208、鉛-206和鉛-207。而鉍-209是第四條衰變鏈錼衰變鏈的倒數第二個子核種,會衰變成穩定的鉈-205。[41]
其餘11種天然放射性元素由於半衰期較短,從地球形成至今早已全部衰變殆盡,因此現今都是作為地殼中釷或鈾的衰變產物或鈾的分裂產物生成的。其中5種(釙、氡、鐳、錒和鏷)是釷和鈾較普遍的衰變產物,而剩下6種元素(鎝、鉕、砈、鍅、錼和鈽)在自然界中僅痕量存在:砈和鍅只存在於鈾衰變鏈和錒衰變鏈的非常小的分支中,不但難以被生成,半衰期也極短,會很快衰變成其他元素;而原子序數較小的鎝和鉕是由鈾-238的自發分裂以及由鉬/釹分別發生中子俘獲而產生;至於超鈾元素錼和鈽則只能由鈾發生中子俘獲而生成。由於這6種元素在自然界中極端稀有,因此除了鍅之外最初都是透過人工合成的方法發現的,直到後來才發現它們也存在於自然界中。[42]鑑於這6種元素在自然界中存量極為稀少,從天然礦石中提取它們並不實際,所以通常還是由人工合成的方式生產這些元素。因此,它們在部分週期表中仍被標記為人造元素。[43]
原子序為95以上的放射性元素都不存在於自然界中,所有同位素都是人造的,稱為人工合成元素或人造元素。[44][45]這些放射性元素的半衰期與地球的年齡相比過短,不但早已全部衰變殆盡,現今自然界中也缺乏形成這些重元素的途徑或機制,因此只能由人工合成的方式生產。人工合成元素可以通過核反應爐或粒子加速器等設備來合成。[46]
另外,有些元素除了穩定同位素外還具有天然存在的放射性同位素,例如鈹-10、碳-14、鋁-26、氪-81等宇生放射性核種和鉀-40、銣-87、釤-147等原始放射性核種,但豐度通常比同一元素的穩定同位素來得低。只有極少數天然放射性同位素的豐度高於同一元素的穩定同位素,例如銦-115(豐度95.71%)、錸-187(豐度62.6%)等。
應用
放射性元素的放射性雖然限制了它們在日常生活中的可用性,卻也為它們在醫療、工業、軍事和能源等領域帶來了許多應用:
- 鈾-235和鈽-239具有很高的熱中子分裂截面,屬於可分裂物質,能夠引發核連鎖反應,因此被廣泛用作核反應爐中的核燃料,也用於製造核武器。[47][48][49]
- 醫療領域中會使用到放射性元素作為診斷用的放射性示蹤劑或放射治療用的放射源,例如鎝-99m被廣泛用於斷層掃描[50][51]、砈-211和錒-225等被用作治療癌症的放射源[52][53][54][55]、鐳-223用於抗癌藥物等。[56][57]
- 使用鋂-241[58]、釙-210[59][60][61]、鐳-226[62][63][64]、錒-227[65]等α粒子發射體混合鈹作為中子源,或者使用鉲-252[66]等自發分裂核種作為中子源,在工業領域有許多應用,例如中子水分測定儀、石油、天然氣和金銀礦等之探勘、核反應爐和核武器的啟動源、中子射線照相術和中子活化分析等。[67][68][69][70][71][72]
- 一些強α粒子放射源被用作放射性同位素熱電機的熱源,例如鈽-238、釙-210、鋦-244、錒-227等,作為人造衛星、太空探測器及無人燈塔等設施的電源。[73][74][75][76][77][78]
- 鎝-99、鉕-147和鋂-242m等β粒子發射體可用於製造射線電池。[79][80][81]
- 鋦-244是太空探測器的α粒子X射線光譜儀中最常見的α粒子射源。[82]
- 常見的游離煙霧探測器中使用極微量的鋂-241氧化物作為游離輻射源,可用來偵測煙霧、預防火災。[83]
- 一些放射性元素被少量地添加到手錶、時鐘和儀錶盤等的發光塗料中,塗料中的螢光粉能吸收放射性物質放出的游離輻射而發光。最初,鐳-226被大量用於此目的,但後來被放射性更低的鉕-147等所取代。[84][85]
- 釙-210等α粒子射源在工業上被用於消除照相板、紡織工廠的紙卷、塑膠片和基材(如汽車)上的靜電。[86][87][88][89]
- 利用鉕-147、釙-210、鉲-252等放射源通過樣品的放射線劑量,可用來測量材料的厚度。[90][91][92][93]
Remove ads
釷是少數因為對其放射性的隱憂而在諸多應用中逐漸被淘汰的元素。釷曾廣泛使用於煤氣燈網罩[94]、GTAW焊的鎢釷電極[95]、白熾燈絲等[96],也被用作高品質透鏡玻璃[97]、耐高溫陶瓷等之添加劑[95]和工業化學反應的催化劑等,但這些應用都因為考量到釷及其衰變產物的放射性對環境和人體健康造成的風險而逐漸被其他材料取代。[95][98]不過作為儲量最豐富的放射性元素,人們正在開發以釷取代鈾作為核反應爐燃料的可能性,目前已有數個釷反應爐被建造。(參見釷燃料發電)[99][100]
除了核武器和核燃料之外,鈾還有一些與放射性無關的應用,例如鈾鹽可用作玻璃著色劑(鈾玻璃)[101][102]、相片調色劑[103]、皮革、木材和絲綢的染色劑等,但這些應用也都和釷一樣隨著人們愈發重視放射性對人體和環境的危害後逐漸減少使用。不過乙酸鈾醯目前仍是廣泛用於電子顯微鏡切片標本的標準負染色劑之一。[104]
另外,以鈾-238為主的貧鈾放射性較弱,可作為飛行器的配重塊、放射線療法和工業用放射造影器材的遮蔽物、承裝放射性物質所使用的貨箱等[105],軍事上則常用作穿甲彈和戰車裝甲的材料[106],但依然有可能對人體造成長期的健康隱患。
鐳是另一個隨著放射性的危害廣為人知而快速淡出人類社會的元素。在放射性剛被發現的幾十年間,鐳-226被大量用於手錶、飛機開關、時鐘和儀錶盤等的發光塗料[107],也在醫療上被用作產生氡氣的藥物,而氡氣用於治療癌症。[108][109]甚至還有不肖廠商誇大放射性的「治療能力」,將鐳-226作為牙膏、護髮霜甚至食品和藥物等產品中的添加劑。[110]鐳在產業中的大量使用造成許多民眾因為放射線中毒而留下終身殘疾甚至死亡,知名的例子包括鐳女郎和運動員埃本·拜爾斯。[111][112][113]目前鐳-226在放射治療和發光塗料中的應用已被其他更安全、更容易獲得的放射性核種所取代。[64][84][86]
由於鉍的放射性過於微弱,直到2003年才被科學家檢測出其具有放射性,半衰期超過宇宙年齡的十億倍。[40]因為鉍-209的半衰期極長,其微乎其微的放射性不會對生物造成任何影響(甚至比人體本身的放射性低得多),所以在幾乎所有應用方面中,鉍都被視為穩定的非放射性元素,無須對其進行任何防護措施,而對其放射性的研究純粹是基於學術興趣。[114]鉍一般以化合態用作藥品、顏料和化妝品[115][116][117][118],少部分用作合金材料和鉛的替代品等。[119][120][121][122]
原子序數≥99(鑀以後)的放射性元素由於半衰期很短,非常不穩定,且無法大量生產,因此目前在科學研究之外沒有任何實際用途。[123]
危害
如果因為一些事故、不良的處理或者其他方法,造成放射性物質被釋放到環境中,它們能潛在並引起有害的效應,即放射性污染。如果過分地使用在醫療或生活應用上,使得人體過度暴露於放射線中,也能導致危險,為放射性中毒。放射性元素也能導致電器故障。
參考文獻
參考書目
參見
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
