Quick Facts 外觀, 概況 ...
碳 6C|
|
| 外觀 |
|---|
透明(鑽石)或黑色(石墨)

鑽石(左)和石墨(右)是碳最常見的兩種同素異形體。 |
| 概況 |
|---|
| 名稱·符號·序數 | 碳(Carbon)·C·6 |
|---|
| 元素類別 | 非金屬 |
|---|
| 族·週期·區 | 14·2·p |
|---|
| 標準原子質量 | [12.0096, 12.0116][1] |
|---|
| 電子組態 | [He] 2s2 2p2
2, 4
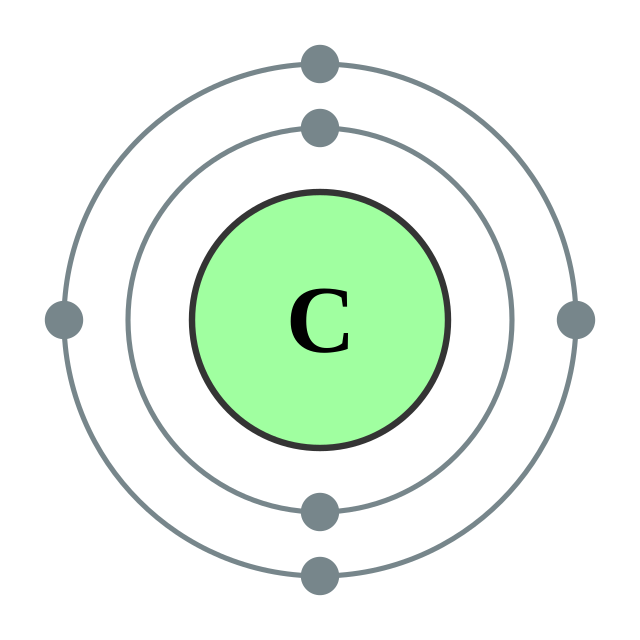 碳的電子層(2, 4) 碳的電子層(2, 4) |
|---|
| 歷史 |
|---|
| 發現 | 古埃及人和蘇美人[2](公元前3750年) |
|---|
| 確認為化學元素 | 安東萬·拉瓦節[3](1789年) |
|---|
| 物理性質 |
|---|
| 物態 | 固體 |
|---|
| 密度 | (接近室溫)
無定形:[4]1.8–2.1 g·cm−3 |
|---|
| 密度 | (接近室溫)
鑽石:3.515 g·cm−3 |
|---|
| 密度 | (接近室溫)
石墨:2.267 g·cm−3 |
|---|
| 昇華點 | 3915 K,3642 °C,6588 °F |
|---|
| 三相點 | 4600 K(4327 °C),10800[5][6] kPa |
|---|
| 熔化熱 | 117(石墨) kJ·mol−1 |
|---|
| 比熱容 | 6.155(鑽石)
8.517(石墨) J·mol−1·K−1 |
|---|
| 原子性質 |
|---|
| 氧化態 | 4, 3[7], 2, 1[8], 0, −1, −2, −3, −4[9] |
|---|
| 電負度 | 2.55(鮑林標度) |
|---|
| 游離能 | 第一:1086.5 kJ·mol−1
第二:2352.6 kJ·mol−1
第三:4620.5 kJ·mol−1
(更多) |
|---|
| 共價半徑 | 77(sp³), 73(sp²), 69(sp) pm |
|---|
| 范德華半徑 | 170 pm |
|---|
 碳的原子譜線 碳的原子譜線 |
| 雜項 |
|---|
| 晶體結構 | 鑽石
(鑽石,透明)
六方
(石墨,黑色) |
|---|
| 磁序 | 反磁性[10] |
|---|
| 熱導率 | 900-2300(鑽石)
119-165(石墨) W·m−1·K−1 |
|---|
| 膨脹係數 | (25 °C)0.8(鑽石)[11] µm·m−1·K−1 |
|---|
| 聲速(細棒) | (20 °C)18350(鑽石) m·s−1 |
|---|
| 楊氏模量 | 1050(鑽石)[11] GPa |
|---|
| 剪切模量 | 478(鑽石)[11] GPa |
|---|
| 體積模量 | 442(鑽石)[11] GPa |
|---|
| 泊松比 | 0.1(鑽石)[11] |
|---|
| 莫氏硬度 | 10(鑽石)
1-2(石墨) |
|---|
| CAS編號 | 7440-44-0 |
|---|
| 同位素 |
|---|
主條目:碳的同位素
|
Close
 提示
提示:此條目頁的主題不是
炭。
碳(英語:Carbon;拉丁語:Carbonium,意為「煤炭」),是一種化學元素,化學符號為C,原子序數為6,原子量為7001120110000000000♠12.011 u,位於元素週期表中的IV A族,屬於非金屬。每個碳原子有四顆能夠進行鍵合的電子,因此其化合價通常為4。自然產生的碳由三種同位素組成:12C和13C為穩定同位素,而14C則具放射性,其半衰期約為5730年。[12]碳是少數幾個自遠古就被發現的元素之一(見化學元素發現年表)。[13]
碳的同素異形體有數種,最常見的包括:石墨、鑽石及無定形碳。[14]這些同素異形體之間的物理性質,包括外表、硬度、電導率等等,都具有極大的差異。在正常條件下,鑽石、碳奈米管和石墨烯的熱導率是已知材質中最高的。
所有碳的同素異形體在一般條件下都呈固態,其中石墨的熱力學穩定性最高。它們不易受化學侵蝕,甚至連氧都要在高溫下才可與其反應。碳在無機化合物中最常見的氧化態為+4,並在一氧化碳及過渡金屬羰基錯合物中呈+2態。無機碳主要來自石灰石、白雲石和二氧化碳,但也大量出現在煤、泥炭、石油和甲烷水合物等有機礦藏中。碳是所有元素中化合物種類最多的,目前有近一千萬種已記錄的純有機化合物,但這只是理論上可以存在的化合物中的冰山一角。[15]
碳的豐度在地球地殼中排列第15(見地球的地殼元素豐度列表),並在全宇宙中排列第4(見化學元素豐度),名列氫、氦和氧之下。由於碳元素極為充沛,再加上它在地球環境下所能產生的聚合物種類極為繁多,因此碳是地球上所有生物的化學根本。[16]




