热门问题
时间线
聊天
视角
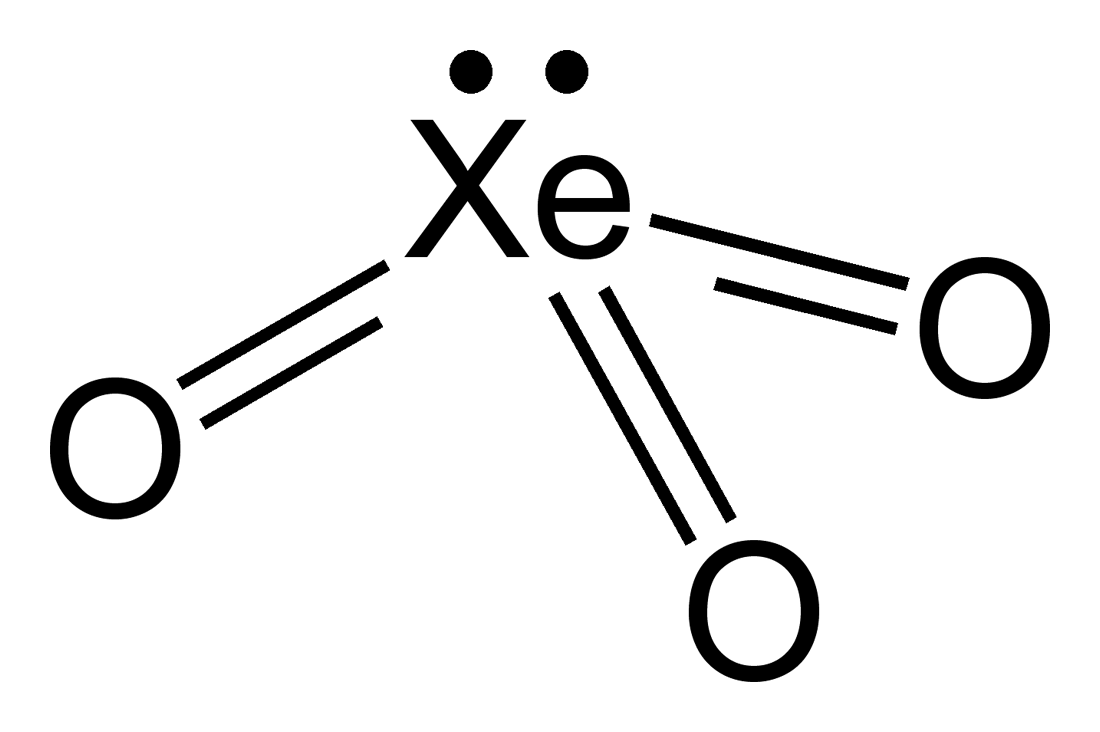
三氧化氙
化合物 来自维基百科,自由的百科全书
Remove ads
三氧化氙是一种不稳定的化合物,其中氙的化合价为+6。它是很强的氧化剂,会缓慢从水中释放氧气,暴露于阳光下会加速反应。它与有机化合物接触时可能会爆炸。它爆炸时会释放氙气和氧气。
Remove ads
化学性质
三氧化氙是一种强氧化剂,可以氧化大多数可以氧化的物质。然而,它的氧化反应缓慢,这降低了它的实用性。[2]
超过 25 °C时,三氧化氙非常容易发生剧烈爆炸:
当三氧化氙溶于水时,会产生酸性的氙酸溶液:
- XeO3(aq) + H2O → H2XeO4 ⇌ H+ + HXeO−
4
该溶液在室温下稳定,没有三氧化氙那样的爆炸性。它可以将羧酸定量地氧化成二氧化碳和水。[3]
三氧化氙溶解在碱性溶液中会形成氙酸盐。HXeO−
4 阴离子是氙酸盐溶液中的主要物种。[4]它们并不稳定,会歧化成高氙酸盐(氧化态+8)和氙气。[5] 含有 XeO4−
6 离子的高氙酸盐可以通过 XeO
3 和氢氧化物溶液反应而成。三氧化氙和KF、RbF和CsF反应,形成通式为 MXeO
3F的化合物。[6]
物理性质
六氟化氙或四氟化氙的水解会产生三氧化氙溶液,通过蒸发可以得到无色的 XeO3 晶体。[7]这些晶体在干燥空气中可稳定数天,但容易从潮湿空气中吸收水分,形成浓溶液。三氧化氙是正交晶系的,晶格参数 a = 6.163 Å、b = 8.115 Å和c = 5.234 Å。它的密度为 4.55 g/cm3。[8]
 |
 |

|
| XeO3晶体一部分的球棍模型 | 空间填充模型 | 氙原子的几何配位 |
危险性
参考文献
外部链接
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads