
Υδροχλωρικό οξύ
From Wikipedia, the free encyclopedia
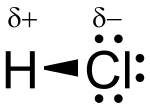
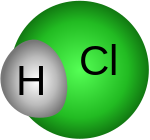
Το υδροχλωρικό οξύ είναι υδατικό διάλυμα του αέριου υδροχλωρίου με το οποίο έχει και τον ίδιο χημικό τύπο, HCl. Είναι ανόργανο ισχυρό οξύ, πολύ διαβρωτικό με πολλές και σημαντικές βιομηχανικές χρήσεις. Προσβάλλει το δέρμα και καταστρέφει κάθε φυτικό ή ζωικό ιστό. Η οσμή του είναι ερεθιστική και αποπνικτική. Το καθαρό υδροχλωρικό οξύ είναι τελείως άχρωμο, αλλά το υδροχλωρικό οξύ του εμπορίου είναι κιτρινωπό επειδή περιέχει προσμίξεις. Τα υγρά του στομάχου περιέχουν υδροχλωρικό οξύ που εκκρίνεται από πολυάριθμους μικρούς αδένες, οι οποίοι βρίσκονται στα τοιχώματά του.
| Το λήμμα παραθέτει τις πηγές του αόριστα, χωρίς παραπομπές. |
| Υδροχλωρικό οξύ | |||
|---|---|---|---|
 | |||
 | |||
 | |||
| Γενικά | |||
| Όνομα IUPAC | Υδροχλωρικό οξύ Υδρογόνο χλωρίδιο (το αέριο) | ||
| Άλλες ονομασίες | Σπίρτο του άλατος, κεζάπι | ||
| Χημικά αναγνωριστικά | |||
| Μοριακή μάζα | 36.46(g/mol) | ||
| Αριθμός CAS | 7647-01-0 | ||
| SMILES | Cl | ||
| InChI | 1/ClH/h1H | ||
| Αριθμός EINECS | 231-595-7 | ||
| Αριθμός RTECS | MW4025000 | ||
| PubChem CID | 313 | ||
| Φυσικές ιδιότητες | |||
| Σημείο τήξης | −27.32 °C (-17.18 °F) (245.83 K) (διάλυμα 38%) | ||
| Σημείο βρασμού | 110 °C (230 °F) (383.15 K) (διάλυμα 20.2%) 48 °C (118.4 °F) (321.15 K) (διάλυμα 38%) | ||
| Πυκνότητα | 1.18 g/mL (μεταβλητή) (τιμή για διάλυμα 36-38% w/w) | ||
| Διαλυτότητα στο νερό | Το αέριο διαλυτό (700 g/L) | ||
| Ιξώδες | 1.9 cP (διάλυμα 31.5%) | ||
| Χημικές ιδιότητες | |||
| pKa | Μεταβλητή, -8.0 (για διάλυμα 37 % w/w) | ||
| Ελάχιστη θερμοκρασία ανάφλεξης | Μη αναφλέξιμο | ||
| Επικινδυνότητα | |||
| Φράσεις κινδύνου | R34, R37 | ||
| Φράσεις ασφαλείας | S1/2, S26, S45 | ||
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |||
Το παλιότερο όνομά του ήταν σπίρτο του άλατος. Το όνομα αυτό το πήρε από την εποχή κατά την οποία παρασκευαζόταν αποκλειστικά και μόνο από το κοινό μαγειρικό αλάτι το οποίο αποτελεί στη φύση άφθονη και φθηνή πρώτη ύλη. Πρώτος περιγράφει γενικά το οξύ ο Άραβας αλχημιστής Γιαμπίρ ιμπν Χαϊάν (Jabir ibn Hayyan) κατά τον 8ο αιώνα. Κατά τη διάρκεια του Μεσαίωνα χρησιμοποιήθηκε από τους αλχημιστές στην αναζήτηση της φιλοσοφικής λίθου[1], και αργότερα από Ευρωπαίους επιστήμονες όπως ο Γιόχαν Ρούντολφ Γκλάουμπερ (Johann Rudolf Glauber), ο Τζόζεφ Πρίστλεϋ (Joseph Priestley) και ο Σερ Χάμφρεϋ Ντέϊβυ (Humphry Davy).
Η παραγωγή του υδροχλωρικού οξέος σε μεγάλη κλίμακα αρχίζει κατά τη Βιομηχανική Επανάσταση και σήμερα χρησιμοποιείται ευρύτατα στη χημική βιομηχανία ως πρώτη ύλη στην παραγωγή πολυάριθμων εμπορικών προϊόντων. Χρησιμοποιείται όμως και σε πολλές άλλες περιπτώσεις όπως για τον καθαρισμό λεκανών των αφοδευτηρίων, για τον καθαρισμό των τοίχων από τις πολλές ασβεστώσεις, για τον καθαρισμό των μετάλλων πριν τον γαλβανισμό τους με ψευδάργυρος, για την παραγωγή ζελατίνης, στην επεξεργασία δέρματος κ.ά.
Από το 1988, το υδροχλωρικό οξύ έχει καταγραφεί στη Σύμβαση των Ηνωμένων Εθνών κατά της παράνομης διακίνησης ναρκωτικών φαρμάκων και ψυχοτρόπων ουσιών ως πρόδρομη ένωση για την παραγωγή της ηρωίνης, της κοκαΐνης και της μεθαμφεταμίνης.