
Gp120
proteïne / Uit Wikipedia, de vrije encyclopedia
Gp120 is een glycoproteïne aan het oppervlak van de Hiv-virusenvelop. Het werd ontdekt door de professoren Tun-Hou Lee en Myron "Max" Essex van de Harvard School of Public Health in 1984.[1] De 120 in de naam komt van zijn molecuulgewicht van 120 kDa. Gp120 is essentieel voor het naar binnengaan van het virus in de cellen, omdat het een cruciale rol speelt bij de hechting aan specifieke membraanreceptoren. Deze receptoren zijn DC-SIGN (Dendritic Cell-Specific Intercellular adhesion molecule-3-Grabbing Non-integrin),[2] heparansulfaat[3] en een specifieke interactie met de CD4-receptor,[4] vooral met T-helpercellen. Binding aan CD4 induceert het begin van een cascade van conformatieveranderingen in gp120 en gp41 die leiden tot de fusie van het virusmembraan met het celmembraan van de gastheer. De binding aan CD4 is voornamelijk elektrostatisch, hoewel er vanderwaalskrachten-interacties en waterstofbruggen zijn.[5]
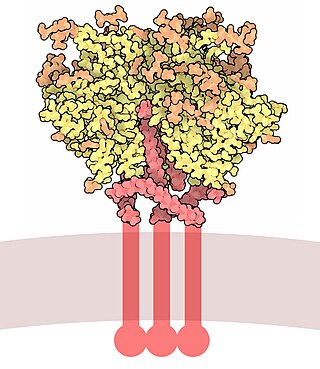

Gp120 wordt gecodeerd door het Hiv-env envelopgen, dat ongeveer 2,5 kb lang is en codeert voor ongeveer 850 aminozuren.[6] Het primaire envelopgenproduct is het eiwit gp160, dat in het endoplasmatisch reticulum door het in het golgicomplex voorkomende protease furine[7] wordt gesplitst in gp120 (~480 aminozuren) en gp41 (~345 aminozuren).[8] De kristalstructuur van de kern van gp120 heeft een buitendomein, een binnendomein met twee uiteinden en een bèta-sheetoverbrugging. Gp120 is verankerd aan de virusenvelop via niet-covalente bindingen met het transmembrane glycoproteïne gp41. Drie gp120's en gp41's worden gecombineerd in een trimeer van hetero-dimeren voor het vormen van envelopspikeiwitten,[9] die voor de hechting aan en het binnendringen van de gastheercel zorgen.
