
Azotasta kiselina
From Wikipedia, the free encyclopedia
Azotasta kiselina (nitritna kiselina) je jedinjenje sa molekulskom formulom HNO2). Ona je slaba i monobazina kiselina koja je poznata samo u rastvoru i u obliku nitritnih soli.[6][7]
Quick Facts Identifikacija, Svojstva ...
| Azotasta kiselina | |
|---|---|
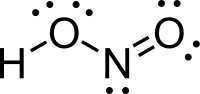 | |
Nitrous acid | |
| Naziv po klasifikaciji | Hidroksidooksidoazot |
| Identifikacija | |
| CAS registarski broj | 7782-77-6 |
| PubChem[1][2] | 24529 |
| ChemSpider[3] | 22936 |
| EINECS broj | 231-963-7 |
| KEGG[4] | C00088 |
| MeSH | Nitrous+acid |
| ChEBI | 25567 |
| ChEMBL[5] | CHEMBL1161681 |
| Gmelin Referenca | 983 |
| 3DMet | B00022 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | HNO2 |
| Molarna masa | 47.013 g/mol |
| Agregatno stanje | bledo plavi rastvor |
| Gustina | Aproksimativno 1 g/ml |
| Tačka topljenja |
Poznata je samo u rastvoru |
| pKa | 3.398 |
| Opasnost | |
| EU-indeks | nije na listi |
| Tačka paljenja | nije zapaljiva |
| Srodna jedinjenja | |
| Drugi anjoni | Azotna kiselina |
| Drugi katjoni | Natrijum nitrit Kalijum nitrit Amonijum nitrit |
| Srodna jedinjenja | Diazot trioksid |
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |
| Infobox references | |
Close
Azotasta kiselina se koristi za pravljenje diazida iz amina. Do toga dolazi nukleofilnim napadom amina na nitrit, reprotonacijom uz pomoć rastvarača, i dvostrukom eliminacijom u vodi. Diazid se zatim oslobađa i daje karben ili karbenoid.