Loading AI tools
রাসায়নিক যৌগ উইকিপিডিয়া থেকে, বিনামূল্যে একটি বিশ্বকোষ
ক্যাডমিয়াম ফ্লোরাইড (CdF2) হল একটি অজৈব যৌগ যা ক্যাডমিয়াম এবং ফ্লোরাইডের মাধ্যমে গঠিত হয়। এটি একটি সাদা, স্ফটিকের কঠিন পদার্থ যা পানিতে অদ্রবণীয়। ক্যাডমিয়াম ফ্লোরাইড একটি বিষাক্ত পদার্থ। এটি বায়ু এবং জলে স্থিতিশীল। এটি বিভিন্ন শিল্প ও বৈজ্ঞানিক প্রয়োগে ব্যবহৃত হয়। ফ্লোরাইড যৌগগুলিও সংশ্লেষী জৈব রসায়নে উল্লেখযোগ্য ব্যবহার রয়েছে।[3]
 | |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
Cadmium fluoride | |
| অন্যান্য নাম
Cadmium(II) fluoride, Cadmium difluoride | |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল) |
|
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৯.২৯৩ |
| ইসি-নম্বর |
|
পাবকেম CID |
|
| ইউএনআইআই | |
কম্পটক্স ড্যাশবোর্ড (EPA) |
|
| |
এসএমআইএলইএস
| |
| বৈশিষ্ট্য | |
| CdF2 | |
| আণবিক ভর | 150.41 g/mol |
| বর্ণ | grey or white-grey crystals |
| ঘনত্ব | 6.33 g/cm3, solid |
| গলনাঙ্ক | ১,১১০ °সে (২,০৩০ °ফা; ১,৩৮০ K) |
| স্ফুটনাঙ্ক | ১,৭৪৮ °সে (৩,১৭৮ °ফা; ২,০২১ K) |
পানিতে দ্রাব্যতা |
4.35 g/100 mL |
Solubility product (Ksp) |
0.00644[1] |
| দ্রাব্যতা | soluble in acid insoluble in ethanol alcohol and liquid ammonia |
চৌম্বকক্ষেত্রের প্রতি সংবেদনশীলতা (χ) |
-40.6·10−6 cm3/mol |
| গঠন | |
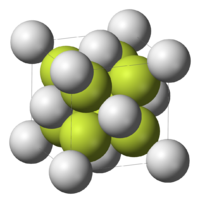
| স্ফটিক গঠন | Fluorite (cubic), cF12 |
| Space group | Fm3m, No. 225 |
| তাপ রসায়নবিদ্যা | |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
-167.39 ± 0.23 kcal. mole-1 at 298.15 (K, C?) |
গিবসের মুক্ত শক্তি (ΔfG˚) |
-155.4 ± 0.3 kcal. mole-1 at 298.15 (K, C?) |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি |    |
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক |
| জিএইচএস বিপত্তি বিবৃতি | H301, H330, H340, H350, H360, H372, H410 |
| জিএইচএস সতর্কতামূলক বিবৃতি | P201, P202, P260, P264, P270, P271, P273, P281, P284, P301+310, P304+340, P308+313, P310, P314 |
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |
PEL (অনুমোদনযোগ্য) |
[1910.1027] TWA 0.005 mg/m3 (as Cd)[2] |
REL (সুপারিশকৃত) |
Ca[2] |
IDLH (তাৎক্ষণিক বিপদ |
Ca [9 mg/m3 (as Cd)][2] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ |
Cadmium chloride, Cadmium bromide Cadmium iodide |
অন্যান্য ক্যাটায়নসমূহ |
Zinc fluoride, Mercury(II) fluoride, Copper(II) fluoride, Silver(II) fluoride, Calcium fluoride, Magnesium fluoride |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
ক্যাডমিয়াম ফ্লোরাইড প্রস্তুত করা হয় ক্যাডমিয়াম ধাতু বা এর লবণের সাথে ফ্লোরিন বা হাইড্রোফ্লোরিক অ্যাসিডের বিক্রিয়া দ্বারা। এটি ক্যাডমিয়াম কার্বনেটকে ৪০% হাইড্রোফ্লোরিক অ্যাসিড দ্রবণে দ্রবীভূত করে, দ্রবণটি বাষ্পীভূত করে এবং ১৫০°C তাপমাত্রায় শূন্যস্থানে শুকিয়ে প্রস্তুত করা যেতে পারে।
এটি প্রস্তুত করার আরেকটি পদ্ধতি হল ক্যাডমিয়াম ক্লোরাইড এবং অ্যামোনিয়াম ফ্লোরাইড দ্রবণ মেশানো, তারপরে ক্রিস্টালাইজেশন। দ্রবণীয় ক্যাডমিয়াম ফ্লোরাইড দ্রবণ থেকে ফিল্টার করা হয়।[4]
ক্যাডমিয়াম সালফাইডের সাথে ফ্লোরিন বিক্রিয়া করে ক্যাডমিয়াম ফ্লোরাইডও প্রস্তুত করা হয়। এই বিক্রিয়া টি খুব দ্রুত ঘটে এবং ব্যবহৃত অন্যান্য বিক্রিয়ার তুলনায় অনেক কম তাপমাত্রায় প্রায় বিশুদ্ধ ফ্লোরাইড তৈরি করে।[5]
ক্যাডমিয়াম ফ্লোরাইড একটি সাদা, স্ফটিকের কঠিন পদার্থ। এটি পানিতে অদ্রবণীয় তবে হাইড্রোফ্লোরিক অ্যাসিডে দ্রবণীয়। এটি একটি বিষাক্ত পদার্থ। এর গলনাঙ্ক 1110°C এবং স্ফুটনাঙ্ক 1748°C। এর ঘনত্ব 6.33 g/cm³।
ক্যাডমিয়াম ফ্লোরাইড বিভিন্ন শিল্প ও বৈজ্ঞানিক প্রয়োগে ব্যবহৃত হয়। এর কিছু গুরুত্বপূর্ণ ব্যবহার হলঃ
ক্যাডমিয়াম ফ্লোরাইড একটি বিষাক্ত পদার্থ। এটি বায়ু এবং জলে স্থিতিশীল হলেও এটি শ্বাসযন্ত্র, ত্বক এবং চোখের জন্য জ্বালাময়। এটি অভ্যন্তরীণভাবে গ্রহণ করলেও বিষাক্ত। ক্যাডমিয়াম ফ্লোরাইডেও ক্যাডমিয়াম এবং ফ্লোরাইড দ্বারা সৃষ্ট একই সম্ভাব্য বিপদ রয়েছে।[7]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.