
Stehiometrija
proračun relativnih količina reaktanata i produkata u hemijskim reakcijama / From Wikipedia, the free encyclopedia
Stehiometrija je stanje i način izračunavanja relativne količine reagensa i proizvoda u hemijskim reakcijama.
Stehiometrija je utemeljena na zakonu održanja mase, gdje je ukupna masa reagenasa jednaka ukupnoj masi proizvoda. To znači da se odnosi između količine reagenasa i proizvoda obično ponašaju kao odnosi pozitivnih cijelih brojeva. To istovremeno govori da ako su poznati iznosi odvojenih reagenasa, onda se može izračunati i iznos proizvoda. Saglasno tome, ako je poznata količina jednog reagensa i količina proizvoda, empirijski se može odrediti jedan od reagenasa, a zatim se može izračunati i iznos drugih reagenasa.[1][2][3][4]
Ovi odnosi se mogu prikazati uravnoteženom jednačinom:
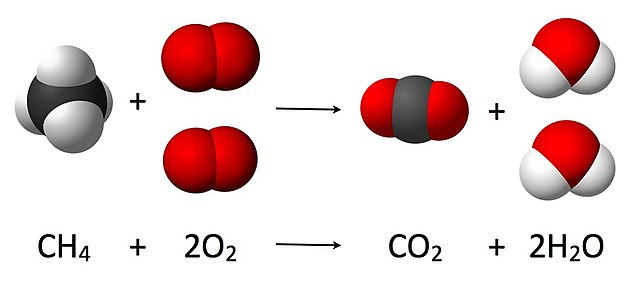
- CH4 + 2 O2 → CO2 + 2 H2O.
Ovdje jedna molekula metana reagira sa dvije molekule plinovitog kisika, pa nastaju jedna molekula ugljik-dioksida i dvije molekule vode. Stehiometrija mjeri ove količinske odnose, a koristi se za određivanje količine proizvoda/reagenasa koji su proizvodeni/potrebni u datoj reakciji. Opisani količinski odnosi među supstancama u hemijskoj reakciji poznati su kao reakcijska stehiometrija. U gornjem primjeru, reakcijska stehiometrija mjeri odnos između metana i kisika koji u međusobnoj reakciji stvaraju ugljik-dioksid i vodu.
Zbog poznatog odnosa molske i atomske težine, dobijeni stehiometrijski koeficijenti mogu se koristiti za određivanje težine u reakciji koja je opisana u uravnoteženoj jednačini. To se zove kompozicijska stehiometrija.
Plinska stehiometrija bavi se reakcijama koje uključuju plinove, a na osnovu poznate temperature, pritiska i zapremine može se pretpostaviti da li je dati uzorak idealan plin. Za plinove, odnos volumena je idealno isti kao i onaj po zakonu o idealnom plinu, ali se odnos mase jedne reakcije mora izračunati iz molekulskih masa reagenasa i proizvoda. U praksi, zbog postojanja izotopa, koriste se molarne mase, umjesto da se izračunava odnos masa.